题目内容
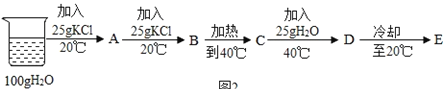
【题目】现有碳酸钠和氯化钠的固体混合样品。由下图实验过程和提供的数据可计算样品中碳酸钠的质量分数约为( )
A.47.5%
B.21.2%
C.70.7%
D.85.6%
【答案】A
【解析】向碳酸钠和氯化钠的固体混合物中,加入盐酸发生的反应为:Na2CO3+2HCl=2NaCl+H2O+CO2↑蒸发时,二氧化碳和水逸出,所以所得固体和原固体质量差为碳酸钠和生成氯化钠的质量差,设混合物中碳酸钠的质量为x,则
Na2CO3+2HCl= | 2NaCl+H2O+CO2↑ | 固体质量差 |
106 | 117 | 11 |
x | 0.55g |
106/x=11/0.55g x=5.3g
样品中碳酸钠的质量分数约为5.3g÷11.15g×100%≈47.5%;
故答案为:A。
根据化学方程式计算分析,利用方程式进行计算时,要先写出有关反应方程式,根据方程式量的关系找出相关物质的相对质量比,再从题中找出已知物质的质量,利用相对质量比与实际质量比相等利出比例式求解,注意溶液之间的反应,参加反应的物质为溶液中的溶质,代入方程式中的质量必须是参加反应或生成的纯净物的质量。

【题目】化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验。同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体。
(1)请写出镁条燃烧的化学方程式______________________________。
(2)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量。有人认为这个反应不遵循质量守恒定律。你认为出现这样实验结果的原因可能是:____________________。
(3)小红按下图装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体。
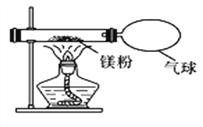
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
【做出猜想】黄色固体是Mg3N2
实验操作 | 实验现象及结论 |
_______________________ | ____________________ |
【实验探究】请设计实验,验证猜想(上表)。
【反思与交流】空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是:_______________________ 。
【题目】某课外小组,用大理石与盐酸反应制取二氧化碳(大理石中杂质不与盐酸反应).甲、乙、丙三同学分别进行实验,实验数据如下(烧杯的质量为25.0g).
烧杯+盐酸 | 大理石 | 充分反应后烧杯+剩余物 | |
甲 | 75.0g | 13.2g | 83.8g |
乙 | 75.0g | 16.0g | 86.6g |
丙 | 95.0g | 13.2g | 103.8g |
若甲、乙、丙三同学中有一名同学所取的大理石和盐酸恰好完全反应,请回答下列问题.
(1) 同学所取的盐酸与大理石恰好完全反应.
(2)计算大理石中碳酸钙的质量分数(计算结果精确到0.1%).