题目内容
【题目】在托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入等质量、等溶质质量分数的稀硫酸,将天平调节至平衡。然后向左盘的烧杯中加入8.4g铁,铁与稀硫酸恰好完全反应。欲使天平恢复平衡,则可向右盘的烧杯中加入( )
A.8.4g 镁
B.8.4g 氧化钙
C.8.4g 锌
D.8.4g 碳酸镁
【答案】A
【解析】
左右两盘加入加入的硫酸质量和浓度都相同,根据反应,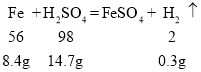 ,8.4g铁生成0.3g氢气,溶液增加的质量为8.4g-0.3g=8.1g,欲使天平恢复平衡,右盘增加的质量也应该是8.1g。或者加入都是8.4g质量的物质后,生成气体的质量也应该是0.3g。硫酸恰好完全反应,所以加入的硫酸溶质质量为14.7g。
,8.4g铁生成0.3g氢气,溶液增加的质量为8.4g-0.3g=8.1g,欲使天平恢复平衡,右盘增加的质量也应该是8.1g。或者加入都是8.4g质量的物质后,生成气体的质量也应该是0.3g。硫酸恰好完全反应,所以加入的硫酸溶质质量为14.7g。
A. 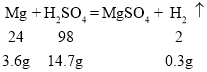 ,加入8.4g金属镁过量,硫酸完全反应,生成了0.3g氢气,右盘溶液的质量增加为:8.4g-0.3g=8.1g,天平恢复平衡。故A符合题意;
,加入8.4g金属镁过量,硫酸完全反应,生成了0.3g氢气,右盘溶液的质量增加为:8.4g-0.3g=8.1g,天平恢复平衡。故A符合题意;
B. 氧化钙遇水反应生成氢氧化钙,没有气体生成,右盘质量增加为8.4g。故B不符合题意;
C. 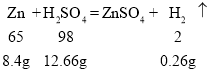 ,该反应中锌全部反应,硫酸过量,生成氢气的质量小于0.3g,右盘溶液质量增加为8.4g-0.26g=8.14g,天平不能恢复平衡。故C不符合题意;
,该反应中锌全部反应,硫酸过量,生成氢气的质量小于0.3g,右盘溶液质量增加为8.4g-0.26g=8.14g,天平不能恢复平衡。故C不符合题意;
D. 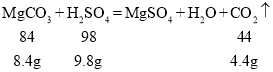 ,该反应中碳酸镁全部反应。硫酸过量,生成气体质量为4.4g,右盘溶液增加的质量为8.4g-4.4g=4.0g,天平不能恢复平衡。故D不符合题意。
,该反应中碳酸镁全部反应。硫酸过量,生成气体质量为4.4g,右盘溶液增加的质量为8.4g-4.4g=4.0g,天平不能恢复平衡。故D不符合题意。
故选A。

 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案【题目】我市某校“绿色”环保小组的同学用精密酸度计测得实验室的甲、乙、丙、丁四种废液的pH如下表。现请你和他们一起实验并回答:
废液 酸碱度 | 甲 | 乙 | 丙 | 丁 |
pH | 6.5 | 11.3 | 7.0 | 2.0 |
(1)各取溶液少许,分别滴入1~2滴无色酚酞试液,能使酚酞试液变红的废液是_________________ 。
(2)实验老师告知:乙、丁分别是未用完的氢氧化钾溶液和稀盐酸。为了防止废液对环境的污染,小聪这一组将丁溶液逐滴滴入乙中,刚好完全反应,此时溶液的pH______7(填“<”、“>”、“=” ) 。该反应的化学方程式为:_____________________ 。
(3)小红这一组在做实验时忘了在乙溶液中滴加酚酞溶液,就滴加了丁溶液,这时立马又滴加了酚酞溶液,发现溶液是无色,此时老师让他们探究此时溶液中的溶质是什么?欢迎你也加入到这一组和他们一起探究,于是他们对溶液中的溶质进行了猜想:猜想1:溶质是氢氧化钾,猜想2:溶质是氯化钾,氯化氢,猜想3: __________ 。经过交流他们认为猜想1不正确你认为不正确的原因:_________。然后他们想了许多方法验证了猜想,请你完成下列实验
所用的方法 | 看到的现象 | 得出的结论 |
向反应的溶液中滴加紫色石蕊溶液 | 猜想2正确 | |
向反应的溶液中加入碳酸钠溶液 | 有较多的气泡产生 | 猜想2正确,写出反应的化学方程式____ |