题目内容
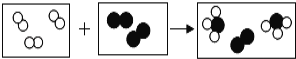
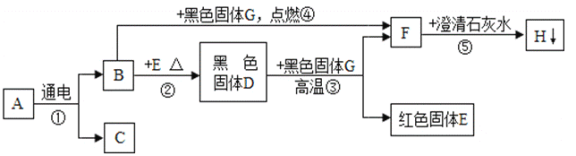
【题目】已知在常温下A为液体,B、C、F是气体; 其中C是密度最小的气体,F是造成温室效应的主要气体;G为黑色固体单质,H是白色难溶于水的固体,它们之间的转变关系如图,请回答下列问题:
(1)写出有关物质的化学式:C是_______; H是_______。
(2)写出反应①的化学方程式_______;该反应的基本反应类型是_______。
(3)写出反应③的化学方程式:_______。
(4)为验证铁、铜、铝三种金属的活动性顺序,可选用的一组物质是(填字母)_______。
A.FeSO4溶液、Cu、AlCl3溶液 B.AlCl3溶液、Fe、Cu
C.CuSO4溶液、Fe、Al D.CuSO4溶液、Fe、AlCl3溶液
【答案】H2 CaCO3 2H2O ![]() 2H2↑+O2↑ 分解反应 2CuO+C
2H2↑+O2↑ 分解反应 2CuO+C![]() Cu+CO2 D
Cu+CO2 D
【解析】
A在通电条件下分解生成B和C,故A为水,水通电分解生成氢气和氧气,C是最轻的气体,则C为氢气,则B为氧气,F是造成温室效应的主要气体,则F为二氧化碳,G为黑色固体单质,在氧气中能燃烧生成二氧化碳,故G为碳;二氧化碳与石灰水反应生成碳酸钙沉淀,故H为碳酸钙;E为红色固体,则E为铜;铜与氧气在加热的条件下生成氧化铜,故D为氧化铜,D氧化铜和黑色固体G在高温条件下反应生成铜和二氧化碳。
(1)由上述分析可知:C是 H2,H是CaCO3;
(2)反应①水分解生成氢气和氧气的过程,方程式为:2H2O![]() 2H2↑+O2↑,该反应的特征是“一变多”为分解反应;
2H2↑+O2↑,该反应的特征是“一变多”为分解反应;
(3)反应③为氧化铜和碳反应的过程,2CuO+C![]() 2Cu+CO2↑;
2Cu+CO2↑;
(4)A、铜和硫酸亚铁溶液、氯化铝溶液都不反应,无法判断铁和铝的活泼性,故错;
B、Cu、Fe均不能置换出AlCl3溶液中的铝,无法判断铁、铜的金属活动性,故错;
C、硫酸铜溶液和铁、铝都反应,无法判断铁和铝的活泼性,故错;
D、Fe、CuSO4溶液、AlCl3溶液,铁与CuSO4溶液反应,与AlCl3溶液不反应,能判断三种金属的活动性顺序,故对。

【题目】某实验小组用石墨做电极进行电解水实验,为增加导电性,改用Ca(OH)2饱和溶液进行电解,实验时除两个电极均有气泡冒出外,溶液中还出现了白色浑浊,该小组对白色浑浊出现的原因进行了如下探究。
(猜想与假设)
① 溶液温度升高导致Ca(OH)2析出而出现白色浑浊。
② 水减少导致Ca(OH)2析出而出现白色浑浊。
③ 与石墨电极有关。
(查阅资料)
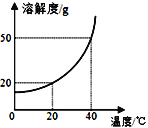
① Ca(OH)2的溶解度:20℃时为0.16 g,100℃时为0.07 g。
② 在加热条件下铜能与氧气反应生成黑色的氧化铜。铜与稀硫酸不反应;氧化铜能与稀硫酸反应。
(进行实验)
实验 | 实验装置 | 主要实验操作 | 实验现象 |
1 | 取20mLCa(OH)2 饱和溶液加热至沸腾 | 溶液中未出现白色浑浊 | |
2 |
| 取Ca(OH)2饱和溶液于烧杯中,加5 ml水,通电3 min | 烧杯中溶液体积几乎无明显变化,溶液中明显出现白色浑浊 |
3 | 更换石墨电极为铜电极,取Ca(OH)2 饱和溶液于烧杯中,通电3 min | 与电源正极相连的铜电极变黑,溶液中未出现白色浑浊 |
(解释与结论)
(1)实验1得出的结论是_______。
(2)实验2通电3 min后得到的溶液为_______(填“饱和”或“不饱和”)溶液。
(3)猜想与假设②不成立,依据的现象是_______。
(4)实验3中更换石墨电极为铜电极的目的是_______。
(反思与评价)
(5)为除去实验3中铜电极上的黑色物质,需要的试剂是______。
(6)通过探究过程,用石墨做电极进行实验时,Ca(OH)2溶液中出现白色浑浊的原因是_______。