题目内容
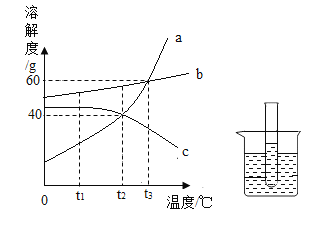
【题目】往稀盐酸和氯化钡的混合溶液中逐滴加入碳酸钠溶液直至过量,根据实验数据绘制下图所示的曲线,下列说法正确的是

A.a到b段有沉淀产生
B.b、d两点的溶质种类均为三种
C.b至c段,溶液中水的质量不变
D.c点存在的微粒为氯离子、钠离子、水分子
【答案】D
【解析】
往稀盐酸和氯化钡的混合溶液中逐滴加入碳酸钠溶液直至过量,先发生盐酸和碳酸钠反应,生成氯化钠、水和二氧化碳,再发生氯化钡与碳酸钠反应,生成碳酸钡沉淀和氯化钠。
A、a到b段发生的反应是盐酸和碳酸钠反应,有气泡产生,没有沉淀产生,A不正确;
B、b点是盐酸与碳酸钠刚好反应完,溶液中溶质有氯化钠和氯化钡两种,d点氯化钡与碳酸钠已反应完且碳酸钠过量,溶液中溶质有氯化钠和碳酸钠两种,B不正确;
C、b至c段是不断加入碳酸钠溶液与氯化钡反应,生成碳酸钡和氯化钠,加入碳酸钠溶液中有水,故溶液中水的质量不断增加,C不正确;
D、c点是碳酸钠与氯化钡刚好完全反应,溶液中溶质只有氯化钠,则存在的微粒为氯离子、钠离子、水分子,D正确。故选D。

【题目】酸碱中和反应是初中常见的反应。
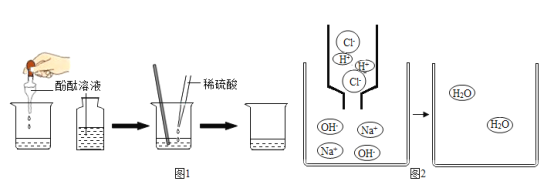
(1)写出上述反应的化学方程式_____;
(2)在氢氧化钠溶液中滴加盐酸,恰好完全反应时其微观示意图如图2,请在图中画出反应后溶液中存在的粒子_____。
(3)用硫酸代替盐酸也可以进行上述实验,取相同浓度(单位体积内含有酸的分子数相同)的硫酸与盐酸,探究与NaOH溶液发生上述反应所需酸的用量:
实验编号 | 酸的种类 | NaOH溶液的体积 | 反应温度/℃ | 溶液褪色时酸的用量/mL |
① | 硫酸 | 10mL | 25 | 2 |
② | 盐酸 | 10mL | 25 | 4 |
③ | 盐酸 | 10mL | 45 | 5 |
在上述几组实验中,我们同时还需要控制的一个变量是:_____,相同条件下,所需的硫酸溶液更少,原因是相同浓度相同体积时,硫酸溶液含有更多的_____(用化学用语表达),比较②和③发现:其他条件不变,温度升高时,要使溶液褪色需要加入更多的盐酸,原因最可能是_____。
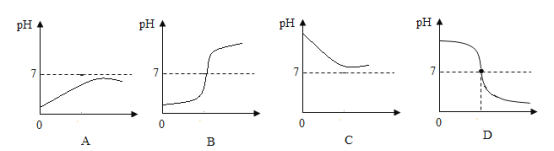
(4)小明同学想调换一下试剂加入的顺序,他先在烧杯中盛10mL稀盐酸,加入几滴酚酞溶液后,用滴管逐滴加入氢氧化钠溶液,并不断搅拌,最终溶液变红,下列曲线能够表示这一过程中溶液pH值变化的是(____)
【题目】能源、环境与化学有着非常密切的联系。
(1)煤石油天然气属于_______________(填“可再生”或“不可再生”)能源。
(2)CO也是一种常见的燃料,它燃烧时发生反应的化学方程式为_______________。由于CO有毒,故为了保证CO完全燃烧,通入的氧气与一氧化碳的质量比的范围是_______________。
(3)氢气作为最清洁能源的优点是_______________。(填一条即可)
(4)下表是我国部分城市空气质量周报。
城市 | 北京 | 天津 | 上海 | 重庆 | 贵阳 |
污染指数 | 93 | 85 | 72 | 120 | 25 |
首要污染物 | 可吸入颗粒物 | 可吸入颗粒物 | NO2 | SO2 | 可吸入颗粒物 |
最容易出现酸雨的城市是______________;为减少该城市酸雨的产生 ,可采取的措施是________________。