题目内容
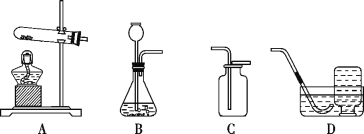
【题目】某化学小组选用以下装置和药品进行探究实验:
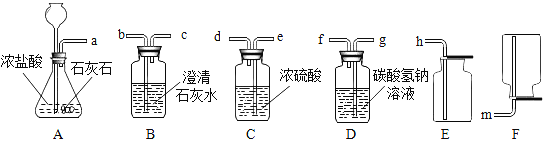
(1)发生装置选择时需要考虑的因素是__________________________________________________
(2)C装置中浓硫酸的作用是_________________________________
(3)若要制取一瓶较为纯净、干燥的CO2,所选用装置的导管接口从左到右的正确连接顺序为:a接______、_______接______、______接_______
【答案】反应物的状态和反应的条件; 干燥二氧化碳 g f e d h
【解析】
(1)根据确定气体发生装置的依据来分析;
(2)根据浓硫酸的性质与用途来分析;
(3)根据制取、除杂、干燥与收集二氧化碳的方法来分析。
(1)气体的制取装置的选择与反应物的状态和反应的条件有关;故填:反应物的状态和反应的条件;
(2)浓硫酸具有吸水性,可以除去二氧化碳中的水蒸气,起到了干燥的作用;故填:干燥二氧化碳;
(3)要制取一瓶较为纯净、干燥的CO2,应先用碳酸氢钠溶液除去二氧化碳中混有的氯化氢气体,再用浓硫酸除去二氧化碳的水蒸气,最后用向上排空气法来收集,注意气体的长进短出;故填:g;f;e;d;h。

【题目】某探究性活动中,甲、乙同学设计并完成了如图所示的实验。(已知![]() )
)
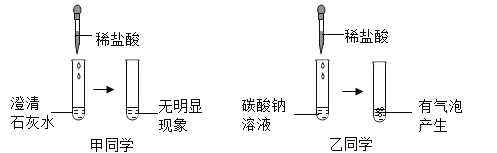
(1)写出甲同学实验中发生反应的化学方程式____________。
(2)反应结束后,甲、乙同学把废液倒入同一废液缸中,观察到废液缸中产生少量的气泡,最终有白色沉淀生成。请回答以下问题:
(Ⅰ)废液缸中最终生成的白色沉淀是_________。
(Ⅱ)甲同学实验后的废液中一定含有的物质是_________。
(3)丙同学从实验(2)的废液缸中取出废液,过滤,对滤液进行了探究。请你帮助丙同学从实验(2)的废液缸中取出废液,过滤,对滤液进行了探究。请你帮助丙同学完成以下探究方案:
探究目的 | 探究步骤 | 实验现象 |
_________ | A.取少量滤液于试管中,滴加过量的稀硝酸 | 产生气泡 |
证明滤液中一定有NaCl | B.向实验A所得溶液中滴加 _________ | 产生白色沉淀 |
(探究结论)该滤液中含有的溶质是碳酸钠和氯化钠。
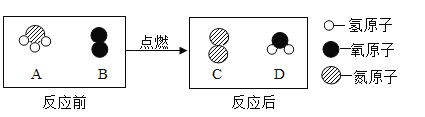
【题目】可燃物R是C、H2、CH4、CO或CH4O中的一种。将一定量的R和氧气置于一个密闭的容器中引燃,测得反应前后各物质的质量如下表:
物质 | R | 氧气 | 二氧化碳 | 水 | 一氧化碳 |
反应前质量/g | m1 | m2 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | m3 | m4 | m5 |
下列叙述正确的是( )
①m1=1/9m4时,R是H2
②m1+m2=m3时,R是C或CO
③ m3:m4=11:9时,R是CH4或CH4O
④8m3/11+8m4/9+4m5/7≥m2
A. ①②③ B. ①③④ C. ②③④ D. ①②③④
【题目】铬(Cr)是一种重要的金属材料,它具有良好的金属光泽和抗腐蚀性,常用来镀在其他金属的表面上,铜、铬、锰、镍组成合金可以制成各种性能的不锈钢。某校化学研究小组对Cr(铬)、Al、Cu的金属的活动性顺序进行探究,过程如下:
(作出假设)对三种金属的活动性顺序提出三种可能的假设:
①Cr>Al>Cu;②Al>Cr>Cu;③__________。
(设计实验)同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象, 记录如下:
金属 | Cr | Al | Cu |
与盐酸反应现 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生激烈,金属迅速溶解 | ___________ |
(控制实验条件)三种金属加入盐酸前都先用纱布将其表面擦光亮,其目的是(_____)
A除去氧化膜,利于直接反应 B使表面光亮,易观察现象 C使金属温度相同,易反应
(得出结论)原假设中正确的是________(选填假设中①、②或③)。写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式:____________________。
(结论应用)(1)根据探究结果,请你预测铬与硫酸铜溶液____________(选填“能”或“不能”)发生反应理由是____________。
(2)铝的化学性质比较活泼,在空气中比铁更易被氧化,但铝制品比铁制品更耐用,是因为铝制品表面有一层致密的氧化铝保护膜,阻止铝进一步被氧化。食醋不宜用铝制品盛放,其原因是_________________。