题目内容
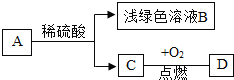
【题目】大庆市某中学化学兴趣小组利用以下装置制备氢气,并验证氢气的性质,按要求回答以下问题:
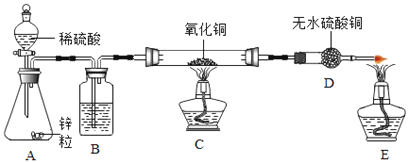
⑴化学实验室现有质量分数为98%的浓硫酸,需配制245g质量分数10%的稀硫酸,配制步骤如下:
①计算:所需质量分数98%的浓硫酸_____g,水的质量为_____g;②量取;③稀释。
⑵该兴趣小组制备氢气的原理为______(用化学方程式表示)。
⑶下列有关实验操作或现象描述不正确的是______(填字母)。
A 实验开始时,应先通入氢气,然后再点燃C处酒精灯
B 点燃C处酒精灯后,D处硫酸铜固体由白色逐渐变为蓝色
C E处酒精灯的作用是点燃未反应的氢气
D 实验结束时,应先停止通入氢气,然后熄灭C处酒精灯
⑷实验结束后,发现部分氧化铜未被还原,已知反应前氧化铜质量为a克,反应结束后混合固体质量为b克,则被氢气还原的氧化铜的质量为______g。
【答案】25 220 Zn+H2SO4=ZnSO4+H2↑ D 5(a-b)
【解析】
(1)①溶液稀释前后溶质的质量不变,设需要98%的浓硫酸的质量为x,则98%x=245g×10%,x=25g,水的质量为:245g-25g=220g。故填:25;220g
(2)稀硫酸与锌粒反应生成硫酸锌和氢气,反应的方程式为:Zn+H2SO4=ZnSO4+H2↑
(3)A.实验开始时,应先通入氢气,然后再点燃C处酒精灯,目的是排净装置内的氢气,以防加热时发生爆炸,故正确;
B.点燃C处酒精灯后,氢气与氧化铜反应生成铜和水,所以D处硫酸铜固体由白色逐渐变为蓝色,故正确;
C.E处酒精灯的作用是点燃未反应的氢气,故正确;
D.实验结束时,应先熄灭酒精灯,然后继续通入氢气直到玻璃管冷却,以防高温生成的铜被重新氧化,故错误。
故选D;
(4)设被还原的氧化铜的质量为x,则

![]() 得x=5(a-b)g
得x=5(a-b)g
故填:5(a-b)g。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案