题目内容
【题目】(14分)水在实验室和日常生活中有很多用途。
I、溶液是日常生活中的常见物质,水是最常用的溶剂。
20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3。请结合图示回答下列问题:
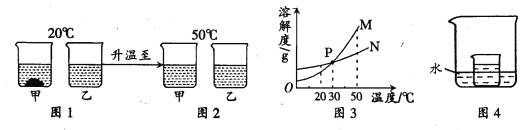
(1)图1中一定为饱和溶液的是
(2)图3中表示乙的溶解度曲线是 ;P点表示的含义是 。
(3)在图4所示的实验中,小烧杯内盛放的是20℃时甲物质的饱和溶液。某同学要使小烧杯内有固体析出时,他应向大烧杯的水中加入下列物质中的 (填字母)。
A.氧化钙 B.氯化钠 C.氢氧化钠 D.硝酸铵
Ⅱ、水在工业生产中也很重要。
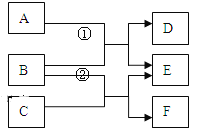
以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。电解饱和食盐水可以得到多种化工产品,主要过程如下:
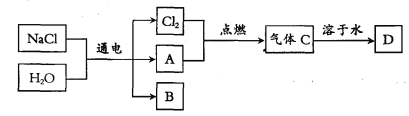
[资料卡:石灰水中的溶质是一种碱——Ca(OH)2]
(4)已知气体A是密度最小的气体,B是一种碱,D是一种酸。写出金属铝和酸D反应生成气体A的化学方程式: 。
(5)B的化学式为 。
(6)工业上电解食盐水是在立式隔膜电解槽中进行,产生的Cl2和气体A在两处逸出并分别收集、储存。
①已知20℃,S(NaCl)=36g,则室温下,68 kg饱和食盐水中溶质的质量为 。
②电解一段时间,当收集到氯气的质量为0.71 kg时,列式计算生成的B的质量 。
③0.71 kg氯气和A完全反应生成气体C,溶于一定量的水中形成酸D。若酸D中的溶质质量分数为36.5%,则其中水的质量为 。
【答案】(1)甲 (2)N 30℃时M和N的溶解度相等 (3)D (4)2Al + 6HCl=2AlCl3 + 3H2↑
(5)①18kg ②0.8kg ③1.27kg
【解析】
试题分析:(1)判断溶液是否饱和的方法:溶液中有未溶解的溶质,故图1中一定为饱和溶液的是甲
(2)根据在20℃时,等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,结果甲溶解的更少,说明在20℃时,甲的溶解度要小于乙的溶解度,故图3中表示乙的溶解度曲线是N,曲线中交点P点表示的含义是:30℃时M和N的溶解度相等
(3)由于甲的溶解度随温度的升高而增大,故要使20℃时甲物质的饱和溶液析出晶体,可以降低温度,硝酸铵溶于水吸收热量,使温度降低,故选D
(4)因为A是密度最小的气体,是氢气,氢气在氯气中燃烧生成气体C为氯化氢,溶于水后得到盐酸,故金属铝和酸D反应生成气体A的化学方程式:2Al + 6HCl=2AlCl3 + 3H2↑
(5)①已知20℃,S(NaCl)=36g,表示在100g水中达到饱和状态溶解的氯化钠质量为36g,故室温下,68 kg饱和食盐水中溶质的质量为18kg
②根据上面的分析可知B是NaOH,然后再根据化学方程式:2NaCl+2H2O通电2NaOH+H2↑+Cl2↑中NaOH与Cl2的质量关系即可求出NaOH的质量
解:设NaOH的质量为x
2NaCl+2H2O通电2NaOH+H2↑+Cl2↑
71
X 0.71 kg
80:71=x:0.71 kg
x=0.8kg
③首先根据化学反应:H2+Cl2点燃2HCl中Cl2与HCl的质量关系,算出HCl的质量,再根据溶质质量分数的计算表达式计算
解:设HCl的质量为x
H2+Cl2点燃2HCl
73
0.71kg x
71:73=0.71kg :x
x=0.73 kg
再设加水的质量为y,列式为:0.73 kg:(0.73 kg+y)=36.5%
y=1.27kg

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案【题目】根据下表中列出的几种常见的气体和空气的性质,可知其中既能用排水法又能用向下排空气法收集的是
项目 | 空气 | A(甲烷) | B(二氧化硫) | C(氨气) | D(氯化氢) |
0℃、101kPa时的密度(g/L) | 1.29 | 0.72 | 2.86 | 0.77 | 1.63 |
20℃、101kPa时1体积水中溶解气体的体积 | / | 0.033 | 40 | 680 | 500 |
【题目】(13分)钠的化合物在日常生活中应用广泛.
(1)碳酸氢钠是发酵粉的成分之一,其俗称是 .
(2)氯化钠是重要的调味品,通过以下化学反应均能生成NaCl.
反应一:钠在氯气中燃烧.反应的化学方程式为 .
反应二:NaOH溶液与稀盐酸反应.关于该反应,下列说法正确的是
A.该反应是中和反应
B.将一定量的稀盐酸逐滴滴入NaOH溶液中,pH不断减小,说明两者发生了反应
C.将一定量的稀盐酸滴入滴有酚酞的NaOH溶液中,溶液仍为红色,说明两者不反应
D.将一定量的稀盐酸与NaOH溶液混合后溶液的pH=7,说明两者发生了反应
E.将NaOH固体放入稀盐酸中,放出热量,说明两者发生了反应
反应三:用Na2CO3溶液和稀盐酸混合.反应的化学方程式为: .
充分反应后的溶液中一定有NaCl,可能有Na2CO3或盐酸.
①为确定反应后溶液中的溶质,同学们进行了如下实验:
步骤I、确定溶液中是否含有盐酸:
甲同学选用了酸碱指示剂中的 试液;
乙同学选用了镁粉,通过实验观察到 ,确定溶液中一定没有盐酸.
步骤II、通过实验确定溶液中含有Na2CO3
②欲从反应后溶液中得到纯净的NaCl,丙同学设计了如下实验方案:
方案 | 加入试剂 | 分离方法 | 方案评价 |
一 | 适量Ba(OH)2溶液 | 过滤、蒸发结晶 | 不可行,理由是: |
二 | 适量的 | 可行 |
(3)(4分)过氧化钠(Na2O2)是供氧设备中常用的供氧剂.韩国“岁月号”沉船事故发生后,
几百名潜水员携带水下供氧设备参与了打捞工作.过氧化钠与水的反应为:2Na2O2+2H2O═4NaOH+O2↑.现将15.6g过氧化钠加入盛有147.6g水(过量)的烧杯中充分反应,直至固体完全消失,不再有气泡产生.
请计算:①反应生成的氧气质量;②反应后所得溶液中溶质的质量分数.(写出计算过程)