题目内容
【题目】化学实验小组同学为研究某公共场所铁制护栏锈蚀的程度,将6.4g已生锈的铁片,放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如图所示(假设铁片除有Fe2O3外,不含其他杂质)。
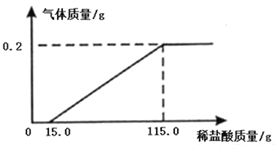
(1)生成氢气的质量为_____g。
(2)所用稀盐酸中溶质的质量分数为多少?______该铁片中Fe2O3的质量分数为多少?____
【答案】0.2 7.3% 12.5%
【解析】
(1)由图可知生成的氢气的质量为0.2g;
(2)设:生成0.2g氢气需要铁的质量为x,所用稀盐酸中溶质的质量分数为y。
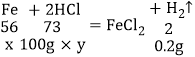
![]() x=5.6g;
x=5.6g;
![]() y=7.3%;
y=7.3%;
铁片中Fe2O3的质量分数=![]() 。
。
答:(1)生成氢气的质量为 0.2g。
(2)所用稀盐酸中溶质的质量分数为7.3%,该铁片中Fe2O3的质量分数为12.5%。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目