题目内容
某班同学按如图所示的实验探究质量守恒定律.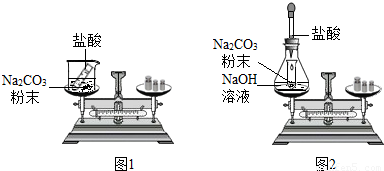
(1)同学们先按图1的方式实验,将盐酸加到碳酸钠粉末中发生反应的化学方程式为______
.该实验中,大家进行了两次称量,有四个小组得到下列数据,其中有问题的两组数据是______(填序号).
| A | B | C | D | |
| 盐酸加入Na2CO3粉末前称量/g | 85.3 | 82.8 | 84.8 | 86.5 |
| 盐酸加入Na2CO3粉末后称量/g | 85.3 | 80.6 | 83.2 | 87.8 |
A.左盘高 B.右盘高 C.保持平衡
该实验中通过化学反应新生成了的物质有______(填序号).
A.HC1 B.CO2 C.Na2CO3 D.NaOH.
【答案】分析:(1)题中探究的是碳酸钠和盐酸反应前后是否平衡,因为碳酸钠与盐酸发生的是化学变化,故无论结果如何,都是遵守质量守恒定律的,之所以天平不平衡的原因是反应中生成了气体的缘故,所以天平会失去平衡;
(2)由于反应在密闭容器中进行,因此容器中所盛的物质的总质量不变;反应有碳酸钠和盐酸产生的二氧化碳,二氧化碳和氢氧化钠反应产生的碳酸钠物质.
解答:解:(1)碳酸钠(Na2CO3)粉末与盐酸(HCl)反应,产生二氧化碳气体、水和氯化钠,反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2;由于实验在敞口的容器中进行,生成的二氧化碳气体逸出,没有收集称量,所以,反应后质量会减轻,而A组数据不变,D组数据增加,故AD两组数据有问题;
(2)由于反应在密闭容器中进行,因此容器中所盛的物质的总质量不变,最终天平的状态是保持平衡
;发生的反应有碳酸钠和盐酸产生的二氧化碳,二氧化碳和氢氧化钠反应产生的碳酸钠物质,故通过化学反应新生成了的物质有二氧化碳和碳酸钠.
故答案为:(1)Na2CO3+2HCl=2NaCl+H2O+CO2↑;AD;
(2)BC.
点评:对于质量守恒定律的理解要注意时所用的物质的质量包括气体、固体和液体,而气体容易被忽略,所以在设计验证质量守恒的实验时要考虑实验是否需要在密闭容器中进行.
(2)由于反应在密闭容器中进行,因此容器中所盛的物质的总质量不变;反应有碳酸钠和盐酸产生的二氧化碳,二氧化碳和氢氧化钠反应产生的碳酸钠物质.
解答:解:(1)碳酸钠(Na2CO3)粉末与盐酸(HCl)反应,产生二氧化碳气体、水和氯化钠,反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2;由于实验在敞口的容器中进行,生成的二氧化碳气体逸出,没有收集称量,所以,反应后质量会减轻,而A组数据不变,D组数据增加,故AD两组数据有问题;
(2)由于反应在密闭容器中进行,因此容器中所盛的物质的总质量不变,最终天平的状态是保持平衡
;发生的反应有碳酸钠和盐酸产生的二氧化碳,二氧化碳和氢氧化钠反应产生的碳酸钠物质,故通过化学反应新生成了的物质有二氧化碳和碳酸钠.
故答案为:(1)Na2CO3+2HCl=2NaCl+H2O+CO2↑;AD;
(2)BC.
点评:对于质量守恒定律的理解要注意时所用的物质的质量包括气体、固体和液体,而气体容易被忽略,所以在设计验证质量守恒的实验时要考虑实验是否需要在密闭容器中进行.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
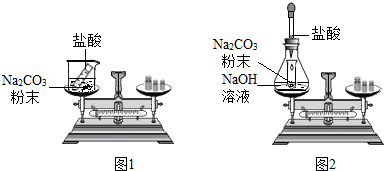
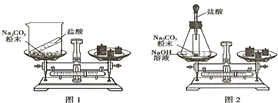 某班同学按如图所示的实验探究质量守恒定律.
某班同学按如图所示的实验探究质量守恒定律. 某校初三(3)班的同学在探究细铁丝在氧气中燃烧的实验中碰到了如下一系列问题,请你帮助解答这些问题:
某校初三(3)班的同学在探究细铁丝在氧气中燃烧的实验中碰到了如下一系列问题,请你帮助解答这些问题: