题目内容
下列是初中化学部分重要的实验或实验装置.请按要求填空:
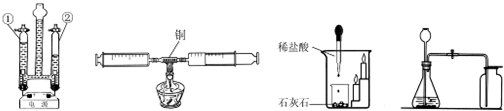
A.水的电解实验 B.测定空气里氧气含量 C.探究二氧化碳性质 D.气体制备装置
(1)A实验玻璃管②中产生的气体是 ;
(2)B实验如果实验数据小于21%,可能原因是 (写一点);
(3)C实验说明二氧化碳具有的性质是 , ;
(4)写出用D装置制取二氧化碳的化学方程式 .
(5)用制取的二氧化碳进行如下实验:

①实验(Ⅱ)中溶液变 色;
②实验(Ⅲ)中加热之后,溶液又变为 色,用化学方程式解释出现此现象的原因 .

A.水的电解实验 B.测定空气里氧气含量 C.探究二氧化碳性质 D.气体制备装置
(1)A实验玻璃管②中产生的气体是
(2)B实验如果实验数据小于21%,可能原因是
(3)C实验说明二氧化碳具有的性质是
(4)写出用D装置制取二氧化碳的化学方程式
(5)用制取的二氧化碳进行如下实验:

①实验(Ⅱ)中溶液变
②实验(Ⅲ)中加热之后,溶液又变为
考点:电解水实验,空气组成的测定,二氧化碳的实验室制法,二氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:实验性简答题
分析:(1)电解水时,正极产生的是氧气,负极产生的是氢气,氧气和氢气的体积比约为1:2;
(2)如果装置漏气,铜不足,反应时间过短,都能够导致实验数据小于21%;
(3)二氧化碳的密度比空气大,不能燃烧,不支持燃烧;
(4)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
(5)二氧化碳能和水反应生成碳酸,碳酸能使石蕊试液变红色;
碳酸的热稳定性差,受热分解生成水和二氧化碳.
(2)如果装置漏气,铜不足,反应时间过短,都能够导致实验数据小于21%;
(3)二氧化碳的密度比空气大,不能燃烧,不支持燃烧;
(4)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
(5)二氧化碳能和水反应生成碳酸,碳酸能使石蕊试液变红色;
碳酸的热稳定性差,受热分解生成水和二氧化碳.
解答:解:(1)A实验玻璃管②中产生的气体是氢气.
故填:氢气.
(2)B实验如果实验数据小于21%,可能原因是装置漏气.
故填:装置漏气.
(3)C实验说明二氧化碳具有的性质是密度比空气大,不能燃烧,不支持燃烧.
故填:密度比空气大;不能燃烧,不支持燃烧.
(4)碳酸钙和稀盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(5)①实验(Ⅱ)中,二氧化碳和水反应生成了碳酸,碳酸能使石蕊试液变红色,因此溶液变红色.
故填:红.
②实验(Ⅲ)中加热之后,碳酸分解生成水和二氧化碳,溶液又变为紫色,碳酸受热分解的化学方程式为:H2CO3
H2O+CO2↑.
故填:紫;H2CO3
H2O+CO2↑.
故填:氢气.
(2)B实验如果实验数据小于21%,可能原因是装置漏气.
故填:装置漏气.
(3)C实验说明二氧化碳具有的性质是密度比空气大,不能燃烧,不支持燃烧.
故填:密度比空气大;不能燃烧,不支持燃烧.
(4)碳酸钙和稀盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(5)①实验(Ⅱ)中,二氧化碳和水反应生成了碳酸,碳酸能使石蕊试液变红色,因此溶液变红色.
故填:红.
②实验(Ⅲ)中加热之后,碳酸分解生成水和二氧化碳,溶液又变为紫色,碳酸受热分解的化学方程式为:H2CO3
| ||
故填:紫;H2CO3
| ||
点评:实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
要使一杯硝酸钾不饱和溶液变为饱和溶液,可采取的方法是( )
| A、加水 | B、不断搅拌 |
| C、升高温度 | D、加入硝酸钾晶体 |
只有一种试剂区别AgNO3、BaCl2、Na2CO3 三种溶液,可选用( )
| A、氯化钙溶液 | B、盐酸 |
| C、稀硝酸 | D、硝酸钾溶液 |




 如图是a、b、c三种物质的溶解度曲线.
如图是a、b、c三种物质的溶解度曲线. 某同学模仿科学家进行粗略测定空气中氧气的体积分数的实验,并提出了自己的实验方法,如图所示,请回答以下问题:
某同学模仿科学家进行粗略测定空气中氧气的体积分数的实验,并提出了自己的实验方法,如图所示,请回答以下问题: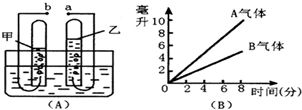 下图是电解水的简易装置,填写下列有关内容.
下图是电解水的简易装置,填写下列有关内容.