题目内容
将氧化铜与足量的木炭粉混合后,高温下充分反应后所得固体的质量减少了2.64g,求:原混合物中氧化铜的质量.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:依据2CuO+C
2Cu+CO2↑可知,该反应中反应前后固体减少的质量就是生成二氧化碳的质量,所以利用方程式中二氧化碳的质量可以求出原混合物中氧化铜的质量
| ||
解答:解:由反应的情况可知该反应中反应前后固体减少的质量就是生成二氧化碳的质量,其质量是2.46g;
设原混合物中氧化铜的质量为x,
2CuO+C
2Cu+CO2↑
160 44
x 2.46g
=
x=8.95g
答:原混合物中氧化铜的质量为8.95g;
设原混合物中氧化铜的质量为x,
2CuO+C
| ||
160 44
x 2.46g
| 160 |
| x |
| 44 |
| 2.64g |
x=8.95g
答:原混合物中氧化铜的质量为8.95g;
点评:此题是对化学方程式计算的考查,解题的关键是分析出生成的二氧化碳的质量,进而依据方程式计算的基本步骤即可解决问题.

练习册系列答案
相关题目
1985年,科学家发现了一种新分子,化学式为C60,下列说法错误的是( )
| A、它是单质 |
| B、它是化合物 |
| C、他的一个分子中含有60个碳原子 |
| D、它是由原子直接构成的物质 |
有A、B、C三种物质各15g,混合加热后,生成新物质D10g,C也增加了10g,A没有剩余;若反应中再没有其他物质生成时,参加反应的A、B的质量比为( )
| A、1:1 | B、3:2 |
| C、1:3 | D、3:1 |
下列物质的用途利用了其物理性质的是( )
| A、糖类和油脂作为人体供能的物质 |
| B、农业上常用熟石灰改良酸性土壤 |
| C、工业上常用一氧化碳作还原剂冶炼金属 |
| D、石墨棒作干电池电极 |
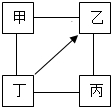 图中,“--”表示相连的物质间在一定条件下可以反应,“→”表示丁在一定条件下可以转化为乙.下面四组选项中,符合图的要求的是( )
图中,“--”表示相连的物质间在一定条件下可以反应,“→”表示丁在一定条件下可以转化为乙.下面四组选项中,符合图的要求的是( )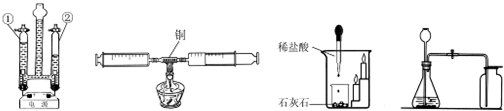


 实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.
实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.