题目内容
用正确的化学反应式填空.
(1)一种淡黄色固体燃烧
(2)有三种生成物的分解反应
(1)一种淡黄色固体燃烧
S+O2
SO2
| ||
S+O2
SO2
| ||
(2)有三种生成物的分解反应
2KMnO4
K2MnO4 +MnO2+O2↑
| ||
2KMnO4
K2MnO4 +MnO2+O2↑
.
| ||
分析:首先根据提供的现象确定发生的化学反应,然后按照书写化学方程式的步骤正确写出相应的化学方程式.
解答:解:(1)淡黄色能燃烧的固体,首先想到硫,硫燃烧生成二氧化硫,化学方程式为:S+O2
SO2
(2)有三种生成物的分解反应比较多,如高锰酸钾分解,碳酸氢铵分解等,高锰酸钾分解生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4
K2MnO4 +MnO2+O2↑.
故答案为:(1)S+O2
SO2
(2)2KMnO4
K2MnO4 +MnO2+O2↑.
| ||
(2)有三种生成物的分解反应比较多,如高锰酸钾分解,碳酸氢铵分解等,高锰酸钾分解生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4
| ||
故答案为:(1)S+O2
| ||
(2)2KMnO4
| ||
点评:根据题意,题目旨在分析所给信息找出反应发生的过程,用化学方程式表示反应.解答此类问题时,主要抓住反应物、生成物和反应条件的辨别和分析,正确书写有关物质的化学式.

练习册系列答案
相关题目
下图所示的是实验室常用的实验装置.
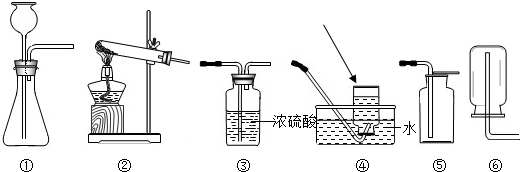
(1)图中所示仪器中,箭头所示名称为 .
(2)加热氯酸钾和二氧化锰固体制取氧气,反应中二氧化锰起 作用,反应的化学反应式为 .其发生装置为 (填序号,下同),收集装置可以选取 .
(3)此实验包括以下操作:①加热;②收集气体;③检查气密性;④装入高锰酸钾;
⑤将导管从水中移出;⑥熄灭酒精灯.正确的操作顺序是 (填序号)
(4)如果选用过氧化氢和二氧化锰制取氧气,优点是 ;
A生成物只有氧气;B不需要加热;C需要加热;D原料易得
(5)研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需的时间.
问题:从上表中能得出哪些结论?(只任写一条)如实验室用过氧化氢和二氧化锰的混合物制氧气,请写出反应式 .
(6)如何证明制取的气体是否为氧气?

(1)图中所示仪器中,箭头所示名称为
(2)加热氯酸钾和二氧化锰固体制取氧气,反应中二氧化锰起
(3)此实验包括以下操作:①加热;②收集气体;③检查气密性;④装入高锰酸钾;
⑤将导管从水中移出;⑥熄灭酒精灯.正确的操作顺序是
(4)如果选用过氧化氢和二氧化锰制取氧气,优点是
A生成物只有氧气;B不需要加热;C需要加热;D原料易得
(5)研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需的时间.
| 浓度 时间(min) 条件 |
30%H2O2 | 15%H2O2 | 5%H2O2 |
| 加入agMnO2 | 0.2 | 0.8 | 2.0 |
| 加入agFe2O3 | 7.0 | 9.0 | 16.0 |
(6)如何证明制取的气体是否为氧气?
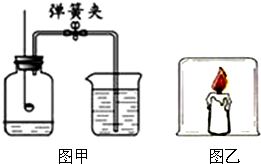 请回答下列问题:
请回答下列问题: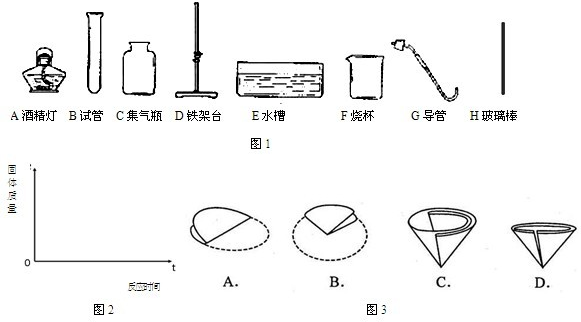
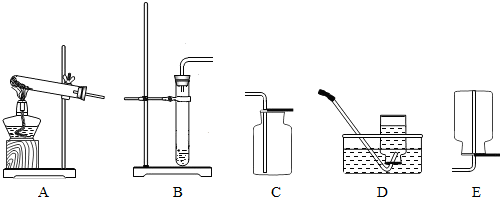
 用来测定空气成分的方法有很多,课本上就是用红磷在空气中燃烧的测定方法.实验过程有:
用来测定空气成分的方法有很多,课本上就是用红磷在空气中燃烧的测定方法.实验过程有: