题目内容
原子序数在1~18之间的四种元素甲、乙、丙、丁,其最外层电子数的总和为13,甲、乙和丙是具有相同电子层数的相邻元素,则丁一定不是( )A.氢
B.氯
C.氧
D.铍
【答案】分析:本题给出的是氢、氯、氧、铍,氢是只有一个质子,核外一个电子;氯是17号,最外层电子数是7;氧是8号,最外层电子数是6;铍是4号,最外层电子数是2.因为甲、乙和丙是具有相同电子层数的相邻元素,甲、乙、丙、丁其最外层电子数的总和为13,因此丁一定不是氧和铍.
解答:解:A、丁是氢的话,甲乙丙分别是硼,碳,氮.或者是铝,硅,磷;不符合题意,故选项错误;
B、丁是氯的话,甲乙丙分别是锂,铍,硼,或者是钠,镁,铝;不符合题意.故选项错误;
C、丁是氧的话,不可能正确,符合题意,故选项正确;
D、丁是铍的话,不可能正确,符合题意,故选项正确;
故选C、D
点评:本考点属于元素的推断题,做本类题型时,要注意题目给出的信息,利用已知条件来解决有关的问题.本题考查了氢、氯、氧、铍四种元素,还要分析最外层电子数,综合性比较强,要认真掌握.本考点主要出现在填空题和实验题中.
解答:解:A、丁是氢的话,甲乙丙分别是硼,碳,氮.或者是铝,硅,磷;不符合题意,故选项错误;
B、丁是氯的话,甲乙丙分别是锂,铍,硼,或者是钠,镁,铝;不符合题意.故选项错误;
C、丁是氧的话,不可能正确,符合题意,故选项正确;
D、丁是铍的话,不可能正确,符合题意,故选项正确;
故选C、D
点评:本考点属于元素的推断题,做本类题型时,要注意题目给出的信息,利用已知条件来解决有关的问题.本题考查了氢、氯、氧、铍四种元素,还要分析最外层电子数,综合性比较强,要认真掌握.本考点主要出现在填空题和实验题中.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
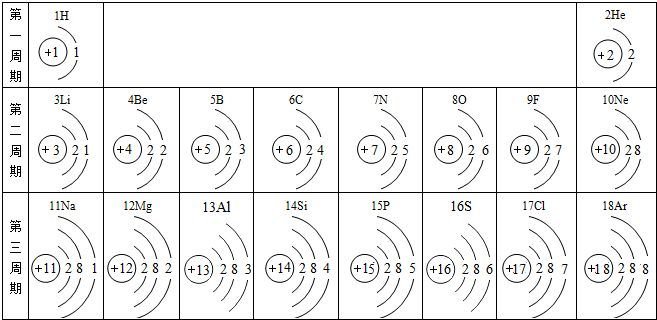
核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题:
 |
 |
(1)在第二周期中,各原子结构的共同之处是 ▲ ;该周期中,各原子核外电子排布的变化规律是 ▲ 。
(2)在第三周期中,元素类型的变化情况是:从左到右由 ▲ 元素过渡到 ▲ 元素,并以稀有气体元素结束。
(3)写出一个核外电子排布与氖原子相同的阳离子:阳离子▲ 。
(4)一般地说,电子层数相同的原子(稀有气体除外),原子的半径随原子序数的递增而减小;最外层电子数相同的原子,原子的半径随电子层数的增加而增大。请比较:氮原子半径▲ 磷原子半径;氧原子半径 ▲ 氟原子半径。(填“>”或“<”)
 (1)在第二周期中,各原子结构的共同之处是
(1)在第二周期中,各原子结构的共同之处是