题目内容
【题目】如图所示变化过程中,对应关系正确的是
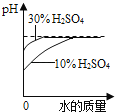
A.稀释等质量的30%H2SO4和10% H2SO4

B.往等质量的Na2CO3和NaHCO3固体中加入足量HCl溶液

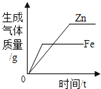
C.将等质量的Mg和Fe投入到足量稀H2SO4中

D.电解水
【答案】B
【解析】A、浓度越大的浓硫酸酸性越大,一开始时30%H2SO4的pH应更小,故A错;
B、碳酸氢钠溶液与盐酸反应的速率更快,设碳酸钠和碳酸氢钠的质量均为1g,则:
NaHCO3+2HCl═NaCl+H2O+CO2↑
84 44
1g ![]() g
g
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
1g ![]() g
g
所以可以判断等质量的碳酸钠和碳酸氢钠,碳酸氢钠反应产生二氧化碳的质量要大,故B正确;
C、镁的活动性比铁强,所以反应速率要快,但是图中显示的是铁的反应速率快,故C错;
D、电解水实验中产生氢气和氧气的质量之比为1:8,故D错.

 春雨教育同步作文系列答案
春雨教育同步作文系列答案【题目】化学兴趣小组的同学在实验室发现一瓶保管不当,盛有无色溶液的试剂瓶,且标签破损(如图),其残缺的标签中只剩下“Na”字样.老师告诉他们,这瓶溶液中的溶质可能是氢氧化钠、氯化钠或碳酸钠.同学们很感兴趣,决定对其成分进行探究.

【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是 (填字母).
A.酸 B.碱 C.盐
【查阅资料】碱性的Na2CO3溶液与中性的CaCl2溶液能发生复分解反应.
【作出猜想】(1)可能是 溶液;(2)可能是Na2CO3溶液;(3)可能是NaCl溶液.
【设计并实验】
实验 | 实验操作 | 主要实验现象 | 实验结论和解释 |
Ⅰ | 取样于试管中,向其中滴加几滴无色酚酞溶液. | 无色溶液变红色 | 该溶液不可能是 溶液.理由是 . |
Ⅱ | 另取样于另一支试管中,向其中滴加足量的 . | 产生大量的气泡 | 该溶液中为碳酸钠.有关反应的化学方程式为: . |
由此,同学们得出结论:该溶液是碳酸钠溶液.
老师指出该结论不严密.理由是:氢氧化钠溶液在空气中敞开放置,发生变质,能产生与实验Ⅰ和Ⅱ相同现象.请写出氢氧化钠溶液在空气中变质的化学反应方程式 .老师指出,不需另取样,只要在实验Ⅰ后的试管中加入足量CaCl2溶液,若观察到 现象,即可说明该溶液中有氢氧化钠.