题目内容
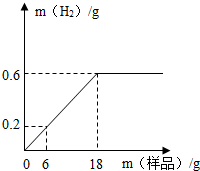 (2013?梅州)为测定某铁粉样品(含少量木炭粉)中铁的含量,往盛有219g该盐酸的烧杯中不断加入铁粉样品,测得生成氢气质量与所加铁粉样品质量的关系如图所示.
(2013?梅州)为测定某铁粉样品(含少量木炭粉)中铁的含量,往盛有219g该盐酸的烧杯中不断加入铁粉样品,测得生成氢气质量与所加铁粉样品质量的关系如图所示.(1)稀盐酸恰好完全反应时,生成氢气的质量为
0.6
0.6
g.(2)6g铁粉样品中含铁单质的质量为
5.6
5.6
g.(3)求稀盐酸中溶质的质量分数(写出计算过程).
分析:(1)从图象可直接读出最终生成氢气的质量;
(2)依据图象可知6g样品生成的氢气质量是0.2g;据此依据方程式的有关计算解答即可;
(3)利用氢气的质量可求出反应的铁和盐酸的质量,而后根据问题计算即可解答;
(2)依据图象可知6g样品生成的氢气质量是0.2g;据此依据方程式的有关计算解答即可;
(3)利用氢气的质量可求出反应的铁和盐酸的质量,而后根据问题计算即可解答;
解答:解:(1)由图象可知最终生成氢气的质量是0.6g;
(2)依据图象可知18g样品生成的氢气质量是0.6g;
设18g样品中铁的质量是x,反应的氯化氢的质量是y
Fe+2HCl═FeCl2+H2↑
56 73 2
x y 0.6g
=
=
x=16.8g y=21.9g
则6g样品中的铁的质量是
=5.6g
(3)故稀盐酸的溶质质量分数为
×100%=10%
故答案为:(1)0.6;(2)5.6;(3)稀硫酸的溶质质量分数是10%;
(2)依据图象可知18g样品生成的氢气质量是0.6g;
设18g样品中铁的质量是x,反应的氯化氢的质量是y
Fe+2HCl═FeCl2+H2↑
56 73 2
x y 0.6g
| 56 |
| x |
| 73 |
| y |
| 2 |
| 0.6g |
x=16.8g y=21.9g
则6g样品中的铁的质量是
| 16.8g |
| 3 |
(3)故稀盐酸的溶质质量分数为
| 21.9g |
| 219g |
故答案为:(1)0.6;(2)5.6;(3)稀硫酸的溶质质量分数是10%;
点评:解答此类问题的根本点在于对反应图象的曲线进行分析,曲线的折点表示此时恰好完全反应.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案
相关题目
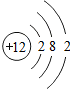 ,则镁原子的核外有
,则镁原子的核外有