题目内容
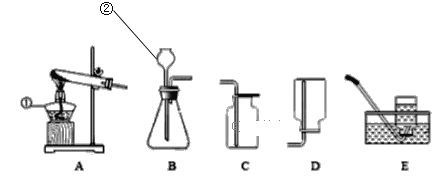
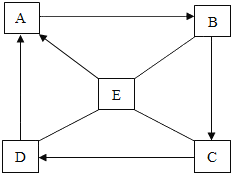
【题目】A~E是初中化学常见的五种物质,有如图的转化关系。A是生命之源。“﹣”表示两端的物质能反应,“→”表示物质间存在转化关系。(部分生成物和反应条件已略去)
(1)写出下列物质的化学式
B_____,D_____。
(2)A生成B反应的基本类型是_____。
(3)写出下列反应的化学方程式:
B→C_____。
C→D_____。
D+E_____。
【答案】Ca(OH)2 Na2CO3 化合反应 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 2NaOH+CO2=Na2CO3+H2O Na2CO3+2HCl=2NaCl+CO2↑+H2O
【解析】
由A是生命之源可确定A为水;水能与可溶性碱对应的金属氧化物反应生成碱,能与非金属氧化物生成对应的酸,结合常见的物质的描述,可推测物质B为常见的金属氧化物氧化钙与水反应生成的常见的碱氢氧化钙;氢氧化钙可与酸性氧化物、酸生成盐和水,而生成的盐都不是常见的盐;与某些盐反应,生成盐和碱,这类反应中可生成常见的碱氢氧化钠;因此,可推测C为氢氧化钠;同样地,根据氢氧化钠的性质与所发生的反应进行推断,氢氧化钠可与二氧化碳反应生成常见的盐碳酸钠和水;可推测D物质为碳酸钠,代入验证,推理成立。
由分析可知:(1) B为氢氧化钙,D物质为碳酸钠,化学式分别为:Ca(OH)2;Na2CO3;
(2)A生成B反应即氧化钙和水生成氢氧化钙,由两种物质反应生成一种物质,属于化合反应;
(3)B→C,纯碱制烧碱,即氢氧化钙与碳酸钠反应生成氢氧化钠和碳酸钙;反应的化学方程式:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
C→D,即由氢氧化钠到碳酸钠,最常见的反应为氢氧化钠与二氧化碳反应生成碳酸钠和水;反应的化学方程式:2NaOH+CO2=Na2CO3+H2O;
D+E,物质E既能与碱物质C氢氧化钠、物质B氢氧化钙,又能与碳酸盐D碳酸钠发生反应,根据常见物质的性质,可推断E为酸,即盐酸或硫酸;所以,D和E的反应即碳酸钠与盐酸或硫酸发生反应生成氯化钠或硫酸钠、水和二氧化碳;反应的化学方程式:Na2CO3+2HCl=2NaCl+CO2↑+H2O(或Na2CO3+H2SO4=Na2SO4+CO2↑+H2O)。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案【题目】实验室有5种白色固体,老师让化学实验小组同学鉴别这些固体.
(1)调查研究
①5种白色固体分别是:NaOH、Na2CO3、CuSO4、Ca(OH)2和NaHCO3.
②查阅资料:小组同学查阅了NaOH、Na2CO3和NaHCO3的一些性质.
性质 | NaOH | Na2CO3 | NaHCO3 |
溶解性 | 20℃时溶解度109g | 20℃时溶解度21.5g 溶解时放热 | 20℃时溶解度9.6g溶解时放热 |
加热 | 不分解 | 不分解 | 发生分解反应,分解产物为碳酸钠、二氧化碳和水. |
(2)实验探究:同学们的探究报告如下,请你帮助完成.
实验步骤 | 实验现象 | 实验结论 | |
第一步:在5支试管中分别放入少量的5种白色固体, 分别标上A、B、C、D、E,然后依次加入一定量的水并振荡. | A、C、D的溶液为无色;B的溶液为浑浊;E的溶液呈蓝色. | B是_____ E是_____ | |
第二步:向上述A、C、D溶液中分别滴加无色的酚酞溶液. | 三支试管中的酚酞溶液均变红. | 结论: _____ | |
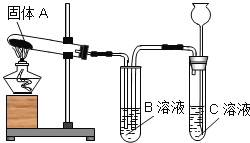
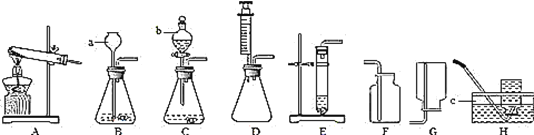
第三步:依据如图装置,对A、B、C进行实验. |
| ||
①加热固体A | B溶液无明显现象. | A是Na2CO3 | |
②待①停止加热后,通过长颈漏斗向C溶液中加入稀盐酸 | C溶液中有气泡产生,B溶液中有气泡逸出并有白色沉淀生成. | B溶液中发生反应的化学方程式为_____ | |
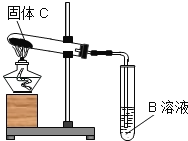
第四步:依据如图装置,对B、C进行实验. |
| 被加热的试管口有无色液滴生成,B溶液中有气泡逸出且溶液变浑浊. | C是_____ 利用排除法得出:D是NaOH |
(3)实验反思:老师引导同学们讨论了上述实验探究过程,进行全面反思,发现实验结论仍有不确定性,不能确定的物质是_____(填化学式);请用物理方法继续鉴别.
实验步骤 | 实验现象和结论 |
_____ | _____ |