题目内容
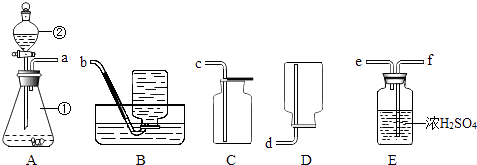
【题目】A、B、C、D、E为初中化学常见五种不同类别的物质,它们之间的关系如图所示(部分物质和反应条件已略去).A、B、C均含有同种金属元素,B→C反应放出大量热,E是相对分子质量最小的单质,则:A的化学式为;反应①和②的化学方程式分别为:、 . 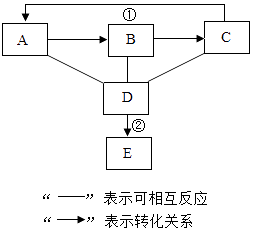
【答案】CaCO3;Ca(OH)2+CO2=CaCO3↓+H2O;2HCl+Zn=ZnCl2+H2↑
【解析】解:A、B、C、D、E为初中化学常见五种不同类别的物质,E是相对分子质量最小的物质,所以E是氢气,A、B、C均含有相同金属元素,B→C反应放出大量热,结合常见的放热反应,A、B、C之间的转化关系和C又会转化成A,猜想A是碳酸钙,B是氧化钙,C是氢氧化钙,A、B、C都会与D反应,D是盐酸,盐酸和活泼金属反应会生成氢气,经过验证,推导正确,所以A是CaCO3 , 反应①是氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O,反应②是锌和盐酸反应生成氯化锌和氢气,化学方程式为:2HCl+Zn=ZnCl2+H2↑. 所以答案是:CaCO3 , Ca(OH)2+CO2=CaCO3↓+H2O,2HCl+Zn=ZnCl2+H2↑.
【考点精析】通过灵活运用书写化学方程式、文字表达式、电离方程式,掌握注意:a、配平 b、条件 c、箭号即可以解答此题.

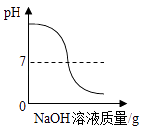
【题目】为了测定某铜锌混合物中锌的质量分数,某同学利用该合金与稀硫酸反应,进行了三次实验,所得相关的实验数据记录如下:
第一次 | 第二次 | 第三次 | |
所取合金的质量/g | 25 | 25 | 50 |
所用稀硫酸的质量/g | 120 | 160 | 100 |
生成氢气的质量/g | 0.4 | 0.4 | 0.4 |
①每一次反应中生成氢气的物质的量是 .
②试计算该铜锌合金中锌的质量分数(写出计算过程).
③从上表数据分析,当所取合金与所用稀硫酸的质量比为时,表明合金中的锌与稀硫酸中的硫酸恰好完全反应.