题目内容
【题目】久置的铜制品表面能生成绿色的铜锈[主要成分为Cu2(OH)2CO3],某化学兴趣小组对铜生锈的条件进行了以下探究。
(提出猜想)根据铜锈的组成元素推测,铜生锈可能是铜与空气中的二氧化碳、水等物质反应的结果。
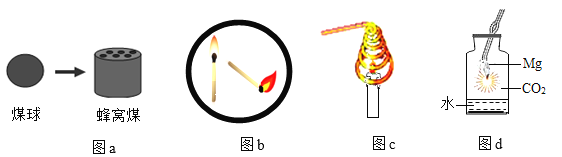
(实验设计)兴趣小组同学取打磨光量的铜丝,设计了如图所示的四个实验。

(现象分析)若干天后,发现只有D瓶中的铜丝出现绿色的铜锈,其他瓶中的铜丝均无铜锈出现。
(1)实验B、C瓶中所使用的蒸馏水是经煮沸后迅速冷却的蒸馏水,其目的是_____。
(2)B瓶与D瓶中的现象对比,可以得出的结论是_____。
(实验结论)由上述四个实验可分析得出,铜生锈是铜与空气中的_____共同作用的结果。
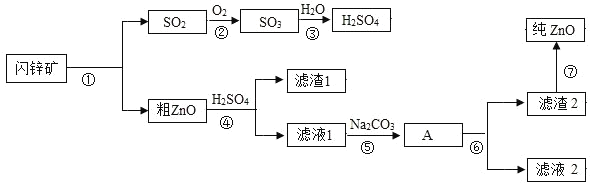
(拓展探究)以锈蚀严重的废铜屑为原料,回收制取纯铜。查阅资料:Cu2(OH)2CO3+2H2SO4═2CuSO4+3H2O+CO2↑;Cu2(OH)2CO3![]() 2CuO+H2O+CO2↑。如图是该兴趣小组设计的两种回收铜的实验方案:
2CuO+H2O+CO2↑。如图是该兴趣小组设计的两种回收铜的实验方案:

(分析评价)
(3)步骤Ⅲ、Ⅳ、Ⅴ都需要进行的实验操作是_____,该操作中玻璃棒的作用是_____。
(4)步骤Ⅱ过程发生反应的化学方程式为_____,此实验开始时要先通一段时间CO再加热,目的是_____。
(5)同一份废铜屑分别通过上述两种方案最终得到的铜的质量:方案一:_____(填“>”或“=”或“<”)方案二:以上两种方案中,方案二优越于方案一,理由是_____(任答一点)。
【答案】除去水中溶解的二氧化碳和氧气 铜生锈需要二氧化碳 二氧化碳、水蒸气和氧气 过滤 引流 CO+CuO![]() Cu+CO2 排尽空气,防止加热CO和空气的混合物引起爆炸 = 无尾气需要处理,不会污染空气
Cu+CO2 排尽空气,防止加热CO和空气的混合物引起爆炸 = 无尾气需要处理,不会污染空气
【解析】
(1)实验B、C瓶中所使用的蒸馏水是经煮沸后迅速冷却的蒸馏水,其目的是:除去水中溶解的二氧化碳和氧气;故填:除去水中溶解的二氧化碳和氧气;
(2)B瓶与D瓶控制的变量为二氧化碳,通过B瓶与D瓶中的现象对比,可以得出的结论是:二氧化碳是铜生锈的必要条件;故填:铜生锈需要二氧化碳。
[实验结论]由上述四个实验可分析得出,铜生锈是铜与空气中的二氧化碳、水蒸气和氧气共同作用的结果;故填:二氧化碳、水蒸气和氧气。
[分析评价]
(3)步骤Ⅲ、Ⅳ、Ⅴ都需要进行的实验操作是:过滤;在过滤的实验中玻璃棒的作用是引流,故填:过滤;引流。
(4)步骤Ⅱ中,一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,化学方程式为:CO+CuO![]() Cu+CO2;此实验开始时要先通一段时间CO再加热,目的是:排尽空气,防止加热CO和空气的混合物引起爆炸;故 :CO+CuO
Cu+CO2;此实验开始时要先通一段时间CO再加热,目的是:排尽空气,防止加热CO和空气的混合物引起爆炸;故 :CO+CuO![]() Cu+CO2;排尽空气,防止加热CO和空气的混合物引起爆炸。
Cu+CO2;排尽空气,防止加热CO和空气的混合物引起爆炸。
(5)上述两种方案中,铜元素既没有增加,也没有减少,同一份废铜屑分别通过上述两种方案最终得到的铜的质量相等;以上两种方案中,方案二优越于方案一,从环保角度分析其理由是:无尾气需要处理,不会污染空气;故填:=;无尾气需要处理,不会污染空气。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案