题目内容
某校九年级(1)班的同学,用氯酸钾和二氧化锰混合加热制取氧气,并把完全反应后的剩余固体进行分离回收,用回收的氯化钾固体配置1000g 5.25%氯化钾溶液,用于浇花.以下是他们设计的实验方案:
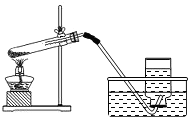
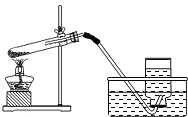
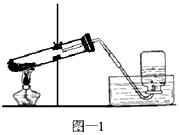
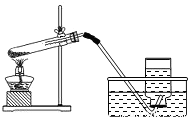
第一步:制取氧气.实验装置如图所示
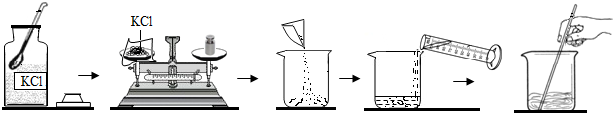
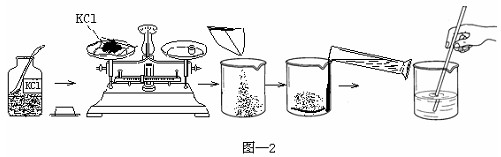
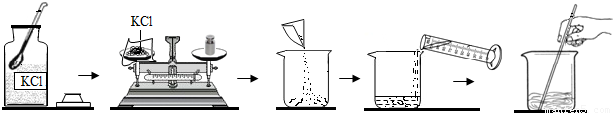
第二步:分离剩余固体,其步骤为:溶解→过滤→蒸发.
第三步:利用回收的氯化钾固体配制1000g 5.25%氯化钾溶液.
全过程如图所示:
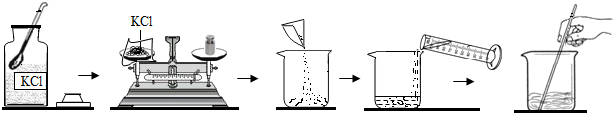
根据上述设计回答:(1)制取氧气的化学反应方程式为:______
(2)指出第一步设计(图)中的两处错误:①______,
②______;
(3)①溶解、过滤、蒸发时都需用到的仪器是______(填序号);
A、酒精灯 B、烧杯 C、玻璃棒 D、漏斗 E、量筒
②用酒精灯加热滤液,进行蒸发操作,当蒸发皿中出现较多固体时,停止加热.利用______.
(4)如果配制的氯化钾溶液中,氯化钾的质量分数小于5.25%,误差的原因有多种,因使用托盘天平和量筒操作不当引起的原因有:
①托盘天平未调零;②砝码和药品放反了;③______;④______(托盘天平和量筒各回答一问).
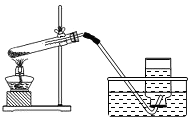
第一步:制取氧气.实验装置如图所示

第二步:分离剩余固体,其步骤为:溶解→过滤→蒸发.
第三步:利用回收的氯化钾固体配制1000g 5.25%氯化钾溶液.
全过程如图所示:

根据上述设计回答:(1)制取氧气的化学反应方程式为:______
(2)指出第一步设计(图)中的两处错误:①______,
②______;
(3)①溶解、过滤、蒸发时都需用到的仪器是______(填序号);
A、酒精灯 B、烧杯 C、玻璃棒 D、漏斗 E、量筒
②用酒精灯加热滤液,进行蒸发操作,当蒸发皿中出现较多固体时,停止加热.利用______.
(4)如果配制的氯化钾溶液中,氯化钾的质量分数小于5.25%,误差的原因有多种,因使用托盘天平和量筒操作不当引起的原因有:
①托盘天平未调零;②砝码和药品放反了;③______;④______(托盘天平和量筒各回答一问).
(1)氯酸钾和二氧化锰混合加热生成氧气和氯化钾,其中二氧化锰作催化剂,生成的气体需加↑,所以化学方程式:2KClO3
2KCl+3O2↑
(2)图中试管的加热方法不正确,应该试管口略向下倾斜(防止水倒流炸裂试管),移动酒精灯灯焰均匀加热,然后用外焰固定在药品部位加热;另外试管内的导气管不能太长,气体不容易导出
(3)①溶解、过滤、蒸发时都需用到的仪器是玻璃棒②蒸发皿中出现较多固体时,停止加热,可以利用蒸发皿的余热使滤液蒸干
(4)对于氯化钾的质量分数小于5.25%,从托盘天平称量药品分析,肯能是①托盘天平未调零②砝码和药品放反③称量时左盘放纸右边不放;从量筒量取溶质水而言,可能是量取水读数时仰视,造成溶质质量偏大,结果溶质质量分数偏小.
故正确答案:
(1)2KClO3
2KCl+3O2↑
(2)①试管口没有略向下倾斜;②进入试管内的导气管太长
(3)①C;②蒸发皿的余热使滤液蒸干.
(4)③称量时左盘放纸右边不放;④量取水读数时仰视
| ||
| △ |
(2)图中试管的加热方法不正确,应该试管口略向下倾斜(防止水倒流炸裂试管),移动酒精灯灯焰均匀加热,然后用外焰固定在药品部位加热;另外试管内的导气管不能太长,气体不容易导出
(3)①溶解、过滤、蒸发时都需用到的仪器是玻璃棒②蒸发皿中出现较多固体时,停止加热,可以利用蒸发皿的余热使滤液蒸干
(4)对于氯化钾的质量分数小于5.25%,从托盘天平称量药品分析,肯能是①托盘天平未调零②砝码和药品放反③称量时左盘放纸右边不放;从量筒量取溶质水而言,可能是量取水读数时仰视,造成溶质质量偏大,结果溶质质量分数偏小.
故正确答案:
(1)2KClO3
| ||
| △ |
(2)①试管口没有略向下倾斜;②进入试管内的导气管太长
(3)①C;②蒸发皿的余热使滤液蒸干.
(4)③称量时左盘放纸右边不放;④量取水读数时仰视

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目