题目内容
在实验室有两瓶无色液体,已知是双氧水和蒸馏水,怎样鉴别它们,请你写出实验的操作步骤、现象和结论。

实验步骤:分别取样,分别加入MnO2
现象:有气泡产生
结论:是双氧水
现象:有气泡产生
结论:是双氧水

练习册系列答案
相关题目
小林觉得你很聪明,是他的良师益友,学完“常见的酸和碱”后,邀请你与他讨论相关的知识:
(1)复习酸的化学性质
由于小林的课堂笔记没做好,有一处未完成,请帮他完成(a)处的空:(a)______.
盐酸、硫酸、食醋具有相似化学性质的原因是因为它们的水溶液中都含有______离子.
(2)复习碱的化学性质
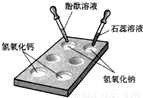
为了复习碱的化学性质小林同学重新做了如图所示的探究实验.请协助小林同学回答:
①使用白色点滴板进行实验的优点是______(答一点);
②氢氧化钠溶液和氢氧化钙溶液都能使无色的酚酞试液变红,是因为在不同碱的溶液中都含有相同的______离子.
③碱除了能和酸碱指示剂显示不同颜色以外,其实还可以与某些非金属氧化物反应,请你帮助小林写出氢氧化钠和二氧化碳反应的化学方程式:______.
(3)如何区别常见的酸和碱溶液实验室现有两瓶无色透明溶液,都没有贴好标签,只知道他们分别是氢氧化钠溶液和稀盐酸中的一瓶,请你设计实验区分好两瓶溶液.______.
(1)复习酸的化学性质
| ①酸与指示剂作用 | 酸溶液能使紫色石蕊溶液变 (a)______ 酸溶液不能使无色酚酞溶液变色 | |
| ②酸与多种活泼金属反应,生成氢气 | Zn+2HCl=ZnCl2+H2↑ | Zn+H2SO4=ZnSO4+H2↑ |
| ③酸与某些金属氧化物作用 | Al2O3+6HCl=2AlCl3+3H2O | … |
| ④… | ||
盐酸、硫酸、食醋具有相似化学性质的原因是因为它们的水溶液中都含有______离子.
(2)复习碱的化学性质
为了复习碱的化学性质小林同学重新做了如图所示的探究实验.请协助小林同学回答:
①使用白色点滴板进行实验的优点是______(答一点);
②氢氧化钠溶液和氢氧化钙溶液都能使无色的酚酞试液变红,是因为在不同碱的溶液中都含有相同的______离子.
③碱除了能和酸碱指示剂显示不同颜色以外,其实还可以与某些非金属氧化物反应,请你帮助小林写出氢氧化钠和二氧化碳反应的化学方程式:______.
(3)如何区别常见的酸和碱溶液实验室现有两瓶无色透明溶液,都没有贴好标签,只知道他们分别是氢氧化钠溶液和稀盐酸中的一瓶,请你设计实验区分好两瓶溶液.______.

实验室有一瓶无色透明液体,只知液体中可能含有盐酸和稀硫酸中的一种或两种,小丽和小华、小敏三位同学为验证该瓶液体,进行了大胆的猜想与实验探究:
【猜想】小丽猜想该瓶液体是盐酸;小华猜想该瓶液体是稀硫酸;
请你推测,小敏的猜想该是______.
【查找资料】硫酸银微溶于水,可看作不溶于水.
【实验】以下是他们三人共同设计的实验方案并进行实验操作,请你补充完整:
写出步骤③反应的化学方程式:______.
【反思评价】
(1)小华对实验步骤③和④提出质疑,他认为将③和④对调,也能得出同样的结论,你同意他的观点吗?______(填“否”或“是”).理由是______.
(2)在进行④骤步时,为什么无需再滴加稀硝酸?因为______.
【猜想】小丽猜想该瓶液体是盐酸;小华猜想该瓶液体是稀硫酸;
请你推测,小敏的猜想该是______.
【查找资料】硫酸银微溶于水,可看作不溶于水.
【实验】以下是他们三人共同设计的实验方案并进行实验操作,请你补充完整:
| 实验操作步骤 | 实验现象 | 实验结论 |
| ①用一支干净试管盛少量的该液体,向试管中滴加______后,再滴加稀硝酸. | ______ | 小华的猜想可能成立 |
| ②另取一支干净试管盛少量该液体,向试管中滴加硝酸银溶液后,再滴加稀硝酸. | 产生白色沉淀 | ______ |
| ③取一支干净试管,盛少量该液体,先向试管中滴加______溶液到不再产生沉淀为止,再滴加稀硝酸. | 产生白色沉淀 | |
| ④用胶头滴管取③的上层清液于另一试管中,滴加硝酸银溶液. | 产生白色沉淀 | 小敏的猜想成立 |
写出步骤③反应的化学方程式:______.
【反思评价】
(1)小华对实验步骤③和④提出质疑,他认为将③和④对调,也能得出同样的结论,你同意他的观点吗?______(填“否”或“是”).理由是______.
(2)在进行④骤步时,为什么无需再滴加稀硝酸?因为______.
 小林觉得你很聪明,是他的良师益友,学完“常见的酸和碱”后,邀请你与他讨论相关的知识:
小林觉得你很聪明,是他的良师益友,学完“常见的酸和碱”后,邀请你与他讨论相关的知识: