题目内容
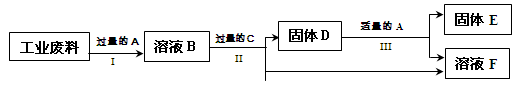
相同质量的Mg、Fe分别与足量的稀盐酸作用,产生H2的质量m(H2)与加入稀盐酸的体积V(稀盐酸)关系如图所示,其中正确的是( )
A. | B.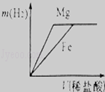 |
C.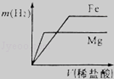 | D.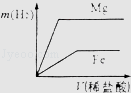 |
D
试题分析:由于两种金属都能和盐酸反应,且盐酸足量,相等质量的金属完全反应时得到的氢气不同,得到的氢气应该是镁对应的更多;根据金属活动性强弱关系镁>铁,可判断镁与稀盐酸反应快,铁与稀盐酸反应慢,即金属镁的反应时间最短最先完成、铁完成的反应消耗时间长;而产生的氢气的质量=
 ×金属质量,二者的化合价相等,镁的相对原子质量小,镁与稀盐酸反应生成的氢气多,故D正确。
×金属质量,二者的化合价相等,镁的相对原子质量小,镁与稀盐酸反应生成的氢气多,故D正确。
练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目