题目内容
【题目】下图是甲转化为丙的微观过程。下列说法错误的是
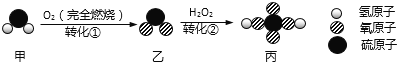
A.转化①中硫、氧元素化合价一定发生改变B.甲、乙均为氧化物
C.转化①中反应的甲与生成的乙的个数比为1:1D.转换②为化合反应
【答案】B
【解析】
A、 转化①中硫化氢和氧气反应生成水和二氧化硫,反应前硫、氧元素化合价为:-2价、0价,反应后硫、氧元素化合价为:+4价、-2价,都发生改变,选项正确;
B、硫化氢中没有氧元素不是氧化物,二氧化硫是由硫、氧两种元素组成的化合物,是氧化物,选项错误;
C、转化①中反应的反应方程式为:3O2+2H2S![]() 2SO2+2H2O,硫化氢与生成的二氧化硫的分子个数比为1:1,选项正确;
2SO2+2H2O,硫化氢与生成的二氧化硫的分子个数比为1:1,选项正确;
D、转换②为二氧化硫和过氧化氢生成丙这一种物质,是化合反应,选项正确。
故选B。

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
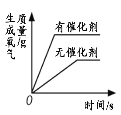
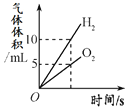
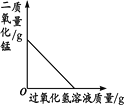
【题目】下列图像能正确反映对应变化关系的是
|
|
|
|
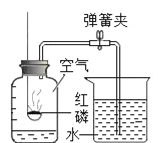
A.用等质量、等浓度的双氧水制取氧气 | B.利用红磷燃烧测定空气中氧气的含量(打开止水夹前) | C.将水通电电解一段时间 | D.向一定量的二氧化锰中加入过氧化氢溶液 |
A. A B. B C. C D. D