题目内容
【题目】如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
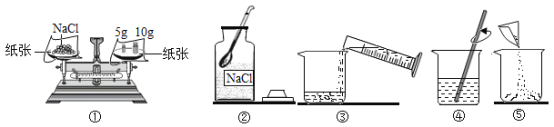
(1)用如图的序号表示配制溶液的正确操作顺序_____。
(2)图②中,有一种塑料仪器,其名称是_____。
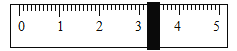
(3)称量NaC时,天平平衡后的状态如图①所示,游码标尺示数见图,则称取的NaCl质量为_____,计算量取水的体积是_____(水的密度为1g/mL)。
(4)经检测该同学配制的溶液溶质质量分数偏小,可能的原因是_____(填序号)。
A.氯化钠固体不纯
B用量筒量取水时俯视读数
C装瓶时有少量溶液洒出
D溶解时烧杯内壁有水珠
【答案】②①⑤③④ 药匙 18.2g 163.8mL AD
【解析】
(1)熟练溶液配制的过程;
(2)熟悉操作过程中所涉及的实验仪器;
(3)根据给出的砝码和游码确定对应的溶质的质量,进而结合溶质的质量分数计算需要的溶剂的质量和体积;
(4)对造成的结果进行针对性分析。
(1)溶液的配制过程为计算﹣称量﹣溶解,所以配制溶液的正确操作顺序 ②①⑤③④;
(2)图②中,有一种塑料仪器,其名称是药匙;
(3)称量NaC时,天平平衡后的状态如图①所示,游码标尺示数见图,则称取的NaCl质量为10g+5g+3.2g=18.2g(游码读刻度尺左侧的数据),则溶液的质量为18.2g÷10%=182g个,需要的水的质量为182g﹣18.2g=163.8g,折合水的体积是 163.8mL;
(4)A、氯化钠固体不纯,即氯化钠的质量少于应该质量,导致配制的溶液溶质质量分数偏小;
B、用量筒量取水时俯视读数,导致液体取少了,配制的溶液溶质质量分数偏大而非偏小;
C、装瓶时有少量溶液洒出,由于溶液已经配好,根据溶液具有均一性可知,质量分数不变;
D、溶解时烧杯内壁有水珠,即水超过了应该质量,配制的溶液溶质质量分数偏小。

 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案