题目内容
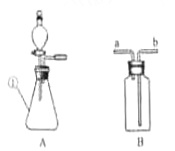
【题目】下图所示,是为了验证稀硫酸化学性质做的 三个实验,回答下列问题。

(1)A实验最终能观察到的现象是 ;
(2)B实验能体现出稀硫酸具有的化学性质是 ;
(3)C实验中发生反应的化学方程式为 ;
(4)将上述实验后所得溶液在烧杯中混合,观察到底部有沉淀层无色溶液,此时利用烧杯中的沉淀再选择适当试剂即可证明C实验中所加BaCl2溶液过量,实验的操作及现象是 。
【答案】(1)溶液呈蓝色;(2)能与活泼金属或金属氧化物反应;(3)H2SO4+BaCl2==BaSO4↓+2HCl;(4)向无色溶液中加入足量稀硫酸,始终有白色固体剩余
【解析】
试题分析:(1)A实验最终氢氧化钠过量,溶液显碱性,故能观察到的现象是溶液呈蓝色;(2)B实验能体现出稀硫酸具有的化学性质是能与活泼金属或金属氧化物反应;(3)氯化钡和稀硫酸发生反应的化学方程式为H2SO4+BaCl2==BaSO4↓+2HCl;(4)证明C实验中所加BaCl2溶液过量,实验的操作及现象是向无色溶液中加入足量稀硫酸,始终有白色固体剩余。

练习册系列答案
相关题目