题目内容
【题目】如图是某空间站能量转化系统局部示意图,其中水电解系统及燃料电池系统中的溶液均采用NaOH溶液。下列有关说法错误的是( )

A.该能量转化系统中的水可以循环使用
B.燃料电池系统中负极产生的气体可以作为燃料使用
C.水电解系统中的溶液采用NaOH溶液,是为了增强水的导电性
D.燃料电池系统产生的能量实际上来自于水
【答案】D
【解析】
A、由转化图可知,该系统中水既可分解也可生成,是循环使用的,说法正确,故不符合题意;
B、燃料电池水电解系统中负极产生的气体是氢气,能燃烧,可以作为燃料使用,说法正确,故不符合题意;
C、水电解系统中的溶液采用KOH溶液,是为了使水的导电性增强,说法正确,故不符合题意;
D、燃料电池系统产生的能量来源于化学反应产生的化学能,属于化学能转变为电能,不是来源于水,说法错误,故符合题意。
故选D。

【题目】实验室制备并收集二氧化碳。
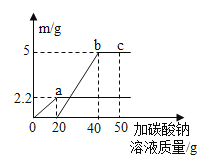
①选用药品。按下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应),产生二氧化碳体积随时间变化曲线如下图所示:
实验编号 | 药品 |
Ⅰ | 块状大理石、10%H2SO4溶液 |
Ⅱ | 块状大理石、7%HC1溶液 |
Ⅲ | 大理石粉末、7%HC1溶液 |
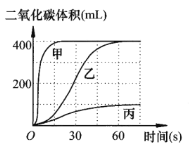
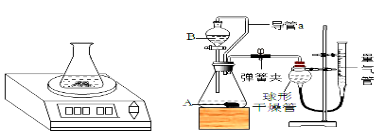
图中丙对应实验______(选填“I”“Ⅱ”或“Ⅲ”)。确定用乙对应的药品制备并收集二氧化碳,相应的化学方程式是 ________;不用甲对应的药品,理由是 ________ 。搭建装置。
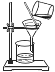
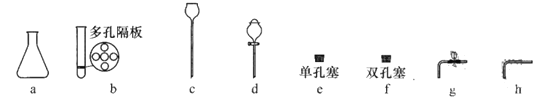
②组装简易启普发生器,应选用________(选填编号)。
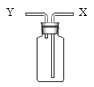
③收集二氧化碳。用下图装置收集时,空气从 _________ (选填“x”或“y”)端排出。
④检验二氧化碳。写出检验时反应的化学方程式。 ___________
【题目】某化学兴趣小组的同学在对蜡烛及燃烧的探究活动中,做了如下实验。
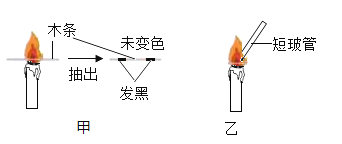
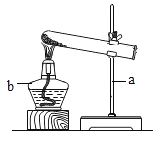
(1)点燃一支白色蜡烛,观察到蜡烛的火焰分为_____层,将一根小木条迅速平放入火焰中,约1秒后取出,现象如图甲,这证明焰心_____;再将一只干燥的烧杯跟在火焰上方,发现罩在火焰上方的烧杯内壁被熏黑并有水珠生成,证明石蜡燃烧发生了_____(选填“物理”或“化学”变化)。
(2)向焰心斜向插入一支细短玻璃管,发现玻璃管中无明显现象(如图乙),在玻璃管的上端管口点燃,上口产生火焰,这说明焰心物质具有的化学性质是_____。同学们对焰心的成分产生了浓厚的兴趣,在老师的指导下,继续进行探究,请你完成其中的步骤。
[提出问题]焰心物质含有什么气体?
[查阅资料]氧气不足时,蜡烛燃烧会生成一氧化碳,一氧化碳能燃烧生成二氧化碳,产生蓝色火焰;石蜡蒸气遇冷会凝结为白色固体。
[猜想和验证](提供用品:火柴、澄清石灰水、小烧杯)
猜想 | 操作 | 现象 | 结论 |
假设①:焰心气体含二氧化碳 | 在未点燃的短玻璃管上口处_____ | _____ | 假设①不成立 |
假设②:焰心气体只含一氧化碳 | 取一较长的细玻璃管,用湿冷毛巾包住中部,将玻璃管下端插入焰心,上端试用火焰点燃 | 玻璃管另一端有蓝色火焰;取下长玻璃管,打开湿毛巾观察到玻璃管内壁无白色固体 | 假设②_____ |
假设③:焰心气体只含石蜡蒸气 | 取一较长的细玻璃管,用湿冷毛巾包住中部,将玻璃管下端插入焰心,上端试用火焰点燃 | 玻璃管另一端口_____;取下长玻璃管,打开湿毛巾观察到_____ | 假设③成立 |
假设④:焰心气体有一氧化碳和石蜡蒸气 | 取一较长的细玻璃管,用湿冷毛巾包住中部,将玻璃管下端插入焰心,上端试用火焰点燃 | 玻璃管另一端口_____;取下长玻璃管,打开湿毛巾观察到_____ | 假设④成立 |
[获得结论]经过同学们的反复实验,确定了焰心气体中含有一氧化碳和石蜡蒸气。
[反思与交流]焰心处之所以会产生一氧化碳,原因是_____。