题目内容
【题目】化学实验是科学探究的重要手段。
(1)某化学小组用如图装置制取气体。
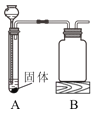
①若实验室用A装置制二氧化碳,反应的化学方程式为_____。
②若检查A装置气密性时,连接好仪器,向长颈漏斗加水之前的操作是什么?____
③若用B装置收集氧气,请将B装置中导管补画完整。_____
④若用B装置排气法收集氧气,请简述如何验满?______
(2)已知甲酸(HCOOH)具有挥发性,在热的浓硫酸中分解生成一氧化碳和水。用如图微型实验装置制取CO,然后用CO还原Fe3O4,并验证气体产物。
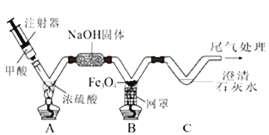
①不考虑尾气处理,此实验过程中发生化学反应一共有_____处。
②写出B中Fe3O4发生反应的化学方程式。______
③实验中验证气体产物的现象是什么?______
(3)为探究一瓶氯化钙溶液的溶质质量分数,取该溶液50g,加入50g碳酸钠溶液,恰好完全反应,所得溶液的质量95克,请计算此氯化钙溶液中溶质的质量分数_____。
【答案】CaCO3+2HCl═CaCl2+H2O+CO2↑ 关闭弹簧夹 ![]() 将带火星的木条放在右导管口处,若木条复燃则证明 6 Fe3O4+4CO
将带火星的木条放在右导管口处,若木条复燃则证明 6 Fe3O4+4CO![]() 3Fe+4CO2 澄清石灰水变浑浊 11.1%
3Fe+4CO2 澄清石灰水变浑浊 11.1%
【解析】
(1)①若实验室用A装置制二氧化碳,是用大理石或石灰石与稀盐酸制取,大理石或石灰石的主要成分是碳酸钙,碳酸钙和盐酸反应生成氯化钙和水以及二氧化碳,反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;
②检查装置气密性时,应先形成密闭体系。检查A装置气密性时,连接好仪器,向长颈漏斗加水之前的操作是关闭弹簧夹(或止水夹,意思答对即可)。
③若用B装置收集氧气,由于氧气的密度大于空气,所以应该用向上排空气法即长进短出,将B装置中导管补画完整为:![]() 。
。
④氧气具有助燃性,能使带火星的木条复燃。若用B装置排气法收集氧气,验满方法为:将带火星的木条放在右导管口处,若木条复燃则证明;
(2)①不考虑尾气处理,此实验过程中发生化学反应有甲酸脱水生成一氧化碳,挥发的甲酸和氢氧化钠反应,一氧化碳和四氧化三铁反应,二氧化碳与氢氧化钙的反应,酒精燃烧两处,所以化学反应一共有6处;
②B中Fe3O4发生反应是一氧化碳和四氧化三铁在高温下生成铁和二氧化碳,反应的化学方程式为Fe3O4+4CO![]() 3Fe+4CO2 ;
3Fe+4CO2 ;
③由于生成二氧化碳,二氧化碳能够使澄清石灰水变浑浊,所以实验中验证气体产物的现象是澄清石灰水变浑浊。
(3)根据质量守恒定律可得,生成的碳酸钙的质量为50g+50g﹣95g=5g;
设:此氯化钙溶液中溶质的质量分数为x
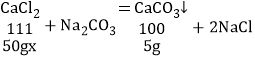
![]() x=11.1%。
x=11.1%。

【题目】实验室有一变质的氢氧化钠样品(样品中只含碳酸钠杂质,且成分均匀),为测量样品中Na2CO3的质量分数,小明进行了如下实验。
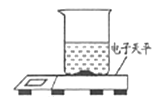
①取质量、大小相同的3个烧杯,分别加入一定质量分数的稀盐酸100克,
②向上述3个烧杯中分别加入3 份质量不同的样品;
③充分反应后,再用电子天平称量烧杯及烧杯内物质的总质量(假设产生的气体完全逸出)。实验数据记录如下:
实验一 | 实验二 | 实验三 | |
反应前稀盐酸+烧杯质量(克) | 150 | 150 | 150 |
反应前固体样品质量(克) | 4 | 8 | 12 |
反应后烧杯内物质+烧杯质量(克) | m | 155.8 | 158.7 |
已知实验中发生的化学反应:NaOH+HCl=NaCl+H2O
Na2CO3+ 2HCl=2NaCl+H2O+ CO2↑
(1)分析表中教据,写出判断实验二中的样品已完全反应的理由__________。
(2)表中的m 值为________。
(3)根据实验二的数据计算样品中Na2CO3的质量分数。
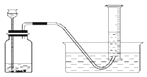
【题目】为了比较甲、乙两种金属的活动性强弱,小明设计了如图实验装置。他取两种金属(表面积相同)各m克,分别加入足量的稀硫酸(相同质量分数)进行反应。在相同条件下测定不同时间内产生氢气的体积,实验记录如下表:
反应时间(秒) | 20 | 40 | 60 | 80 | 100 | 120 | 140 |
甲金属生成氢气的体积(毫升) | 25 | 60 | 95 | 130 | 160 | 170 | 170 |
乙金属生成氢气的体积(毫升) | 30 | 75 | 120 | 150 | 150 | 150 | 150 |
(1)除了图示装置,实验中还需要用到的测量仪器有______。
(2)由实验结果可知:金属活动性较强的是______。
(3)为使得到的实验数据准确,应该从______时开始收集气体。