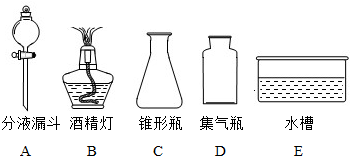
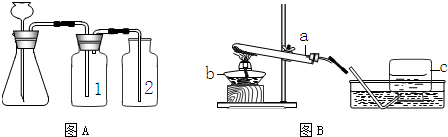
题目内容
学校实验室的废液缸中收集了同学们在实验室制取CO2后的所有废液.小红同学想探究废液中溶质的成分,请你一同参与探究并回答下列问题.[提出问题]废液中的溶质是什么物质?
[作出猜想]小红认为废液中溶质只有CaCl2.
你认为还可能含有的溶质是
[查阅资料]CaCl2溶液呈中性,石灰石中杂质不与稀盐酸反应,也不溶于水.
[实验与结论]
(1)如果要证明你的猜想是正确的,你选择的试剂是
(2)若实验证明你的猜想是正确的,要想使处理后的废液只有CaCl2溶液,应向废液中加入过量的
A.硝酸银 B.碳酸钠 C.碳酸钙 D.氢氧化钙
(3)实验前,实验老师共配制1000g14.6%的稀盐酸,若要将其全部反应掉,至少需要多少克80%的石灰石?实验结束后,搜集所有废液,废液中溶质的质量分数是多少?(写出完整的计算过程,计算结果如算不尽,保留一位小数)
分析:根据题目信息可知,碳酸钙和盐酸反应生成氯化钙和二氧化碳和水,所以反应后的溶液的溶质可能是氯化钙和剩余的反应物,但是碳酸钙是沉淀,因此溶质可能是氯化钙和盐酸.
(1)根据盐酸的酸性即可.
(2)根据盐酸的性质(盐酸和盐反应)即可,也涉及除杂的一些知识.
(3)列出化学方程式计算即可.
(1)根据盐酸的酸性即可.
(2)根据盐酸的性质(盐酸和盐反应)即可,也涉及除杂的一些知识.
(3)列出化学方程式计算即可.
解答:解:碳酸钙和盐酸反应生成氯化钙和二氧化碳和水,所以反应后的溶液的溶质可能是氯化钙和剩余的反应物,但是碳酸钙是沉淀,因此溶质可能是氯化钙和盐酸,故答案为:HCl.
(1)盐酸是酸性,能使紫色石蕊试液变红,这是酸碱指示剂的性质,故答案为:紫色石蕊试液、紫色石蕊试液变红.
(2)这个题有三个要求:①能和盐酸反应,②和盐酸反应的产物必须是氯化钙或者沉淀,③加入的物质也必须是沉淀;因此碳酸钙最合适;碳酸钙和盐酸反应的产物是氯化钙和二氧化碳和水,最后的溶质全部是氯化钙;故答案为:C
(3)HCl的质量是1000×14.6%═146g,设生成的氯化钙质量是X,需要的碳酸钙的质量是Y,二氧化碳的质量是Z.
2HCl+CaCO3═CaCl2+CO2↑+H2O
73 100 111 44
146 y x Z
═
得:X═222g
═
得:Y=200g
═
得:Z=88g
所以石灰石的质量是:200÷80%═250g
反应后溶液的质量是:1000+200-88═1112g
溶液中溶质(CaCl2)的质量分数是:
×100%═20.0%
答:若要将其全部反应掉,至少需要250g克80%的石灰石;废液中溶质的质量分数是20.0%.
(1)盐酸是酸性,能使紫色石蕊试液变红,这是酸碱指示剂的性质,故答案为:紫色石蕊试液、紫色石蕊试液变红.
(2)这个题有三个要求:①能和盐酸反应,②和盐酸反应的产物必须是氯化钙或者沉淀,③加入的物质也必须是沉淀;因此碳酸钙最合适;碳酸钙和盐酸反应的产物是氯化钙和二氧化碳和水,最后的溶质全部是氯化钙;故答案为:C
(3)HCl的质量是1000×14.6%═146g,设生成的氯化钙质量是X,需要的碳酸钙的质量是Y,二氧化碳的质量是Z.
2HCl+CaCO3═CaCl2+CO2↑+H2O
73 100 111 44
146 y x Z
| 73 |
| 100 |
| 146 |
| X |
| 73 |
| 111 |
| 146 |
| Y |
| 73 |
| 100 |
| 146 |
| Z |
所以石灰石的质量是:200÷80%═250g
反应后溶液的质量是:1000+200-88═1112g
溶液中溶质(CaCl2)的质量分数是:
| 222 |
| 1112 |
答:若要将其全部反应掉,至少需要250g克80%的石灰石;废液中溶质的质量分数是20.0%.
点评:这个题需要注意的是溶液的质量计算,盐酸的质量是1000,而不是146;计算时要规范.

练习册系列答案
相关题目