题目内容
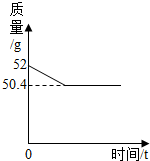 为了测定一瓶过氧化氢溶液中溶质的质量分数,某同学取该溶液50g倒入烧杯中,然后向其中加入2g二氧化锰,烧杯内混合物的质量与反应时间的变化关系如图所示.
为了测定一瓶过氧化氢溶液中溶质的质量分数,某同学取该溶液50g倒入烧杯中,然后向其中加入2g二氧化锰,烧杯内混合物的质量与反应时间的变化关系如图所示.(1)反应完全后产生氧气的质量为
1.6g
1.6g
.(2)欲从反应后的混合物中回收二氧化锰,应进行的操作是
过滤
过滤
、干燥.(3)计算该过氧化氢溶液中溶质的质量分数(结果保留至0.1%).
分析:(1)根据质量守恒定律反应前后减少的质量即为氧气的质量进行解答;
(2)根据二氧化锰不溶于水进行解答;
(3)根据氧气的质量以及质量守恒定律可以计算该过氧化氢溶液中溶质的质量分数.
(2)根据二氧化锰不溶于水进行解答;
(3)根据氧气的质量以及质量守恒定律可以计算该过氧化氢溶液中溶质的质量分数.
解答:解:(1)由质量守恒定律反应前后减少的质量即为氧气的质量,生成的气体的质量为:52g-50.4g=1.6g;故答案为:1.6g;
(2)二氧化锰不溶于水,所以欲从反应后的混合物中回收二氧化锰,应进行的操作是过滤、干燥;故答案为:过滤;
(3)设过氧化氢溶液中溶质的质量为x.
2H2O2
2H2O+O2↑
68 32
x 1.6g
=
x=3.4g
该过氧化氢溶液中溶质的质量分数=
×100%=6.8%
答:该过氧化氢溶液中溶质的质量分数为6.8%.
(2)二氧化锰不溶于水,所以欲从反应后的混合物中回收二氧化锰,应进行的操作是过滤、干燥;故答案为:过滤;
(3)设过氧化氢溶液中溶质的质量为x.
2H2O2
| ||
68 32
x 1.6g
| 68 |
| x |
| 32 |
| 1.6g |
x=3.4g
该过氧化氢溶液中溶质的质量分数=
| 3.4g |
| 50g |
答:该过氧化氢溶液中溶质的质量分数为6.8%.
点评:在解此类题时,首先利用质量守恒定律解出氧气的质量,然后利用方程式中的比例关系解出需要求解的物质的质量.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目