题目内容
轻质碳酸镁2?4H2O)是制取氧化镁、颜料、油漆、日用化妆品的工业原料.【制取轻质碳酸镁】工业上可利用工业副产品氢氧化镁悬浮液(含有的硫酸钠等物质均不与二氧化碳气体反应)采用碳化法制取轻质碳酸镁.
(1)氢氧化镁悬浮液和二氧化碳在一定条件下生成MgCO3?3H2O沉淀,经过滤、洗涤获得纯净的MgCO3?3H2O,该反应的化学方程式为:______,最后加热
MgCO3?3H2O分解生成轻质碳酸镁,化学方程式为
5MgCO3?3H2O
 4MgCO3?Mg(OH)2?4H2O+CO2↑+10H2O.
4MgCO3?Mg(OH)2?4H2O+CO2↑+10H2O.(2)过滤需要用到的玻璃仪器有烧杯、______和______,MgCO3?3H2O沉淀的洗涤干净的标准是取最后一次洗涤液,滴加3滴氯化钡溶液,______,说明已洗净.
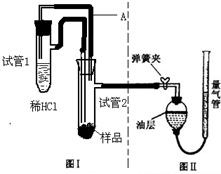
【测定轻质碳酸镁的纯度】轻质碳酸镁与稀盐酸反应生成CO2等物质并放出热量,关系式为 4MgCO3?Mg(OH)2?4H2O~4CO2.如图是实验室测定产品中轻质碳酸镁含量的装置.
(3)检查装置气密性,其中检查图Ⅱ装置气密性的具体操作方法是将水注入图Ⅱ中,弹簧夹夹紧橡胶管,提升量气管高度形成液差,一段时间后,液差______,说明装置气密性良好.
(4)称量2.5g样品装入试管2,在试管1中加入足量的稀盐酸.向图Ⅱ装置中放入水和油,调节左右液面相平,读取量气管的刻度为10ml;将试管1中稀盐酸加到试管2中的具体操作方法是______,待观察试管2中不再产生时,读取量气管的刻度为54mL.
(5)读取量气管内最终液面刻度前,需要进行的操作是______.
(6)实验中量气管的最佳规格是______ml(填“50”、“100”或“150”)
(7)计算样品中4MgCO3?Mg(OH)2?4H2O的质量分数.2?4H2O的相对分子质量为466,常温下CO2的密度约为2.0g/L,要求计算过程,计算结果保留一位小数,)
【交流讨论】
(8)图Ⅰ装置橡胶管A的作用是______,图Ⅱ装置食用油的作用是______;
(9)下列会影响测量结果的事项是______.
A.未冷却就读取量气管中液面刻度
B.原装置中的空气
C.试管1中稀盐酸的体积.

【答案】分析:(1)根据氢氧化镁悬浮液和二氧化碳在一定条件下生成MgCO3?3H2O沉淀的信息回答.
(2)根据回答前一空;根据硫酸钠的性质回答后一空.
(3)根据液体能产生压强考虑回答.
(4)根据装置的结构回答.
(5)根据液柱造成的压强会影响气体体积回答.
(6)根据反应生成气体的体积判断量程.
(7)根据二氧化碳的密度计算出它的质量,再根据关系式 4MgCO3?Mg(OH)2?4H2O~4CO2计算MgCO3?Mg(OH)2?4H2O的质量,最后求质量分数.
(8)根据气压原理回答前一空;根据二氧化碳的溶解性回答后一空.
(9)A、根据气体热胀冷缩的性质判断.
B、根据原装置中的空气与反应后剩余在装置中的气体体积相等判断,
C、根据试管1中稀盐酸的体积变化不大判断.
解答:解:(1)根据信息“氢氧化镁悬浮液和二氧化碳在一定条件下生成MgCO3?3H2O沉淀”右得方程式为Mg(OH)2+CO2+2H2O═MgCO3?3H2O.
(2)过滤操作使用的玻璃仪器有:烧杯、玻璃棒、漏斗;由于硫酸钠能和可溶的钡盐反应生成白色沉淀,如沉淀没洗涤干净,则含有硫酸钠,滴加3滴氯化钡溶液,会生成白色沉淀,否则无沉淀生成.
(3)将水注入图Ⅱ中,弹簧夹夹紧橡胶管,提升量气管高度形成液差,如装置严密,气体压强不会减小,一段时间后,液差不变.
(4)将试管1中稀盐酸加到试管2中的具体操作方法是:倾斜试管1,让稀盐酸从支管口流出进入试管2.
(5)读取量气管内最终液面刻度前,需要进行的操作是调节量气管高度,使左右液面相平,否则管中的液柱能产生压强,对管中的气体进行压缩或拉伸,影响气体的体积测定.
(6)反应生成气体的体积为54mL,50mL的量气管量程太小,150mL的量气管不精确,所以选择100mL的量气管.
(7)解:设样品中4MgCO3?Mg(OH)2?4H2O的质量分数为x
4MgCO3?Mg(OH)2?4H2O~4CO2
466 176
2.5g×x (54-10)×10-3L×2.0g/L

x=93.2%
答:样品中4MgCO3?Mg(OH)2?4H2O的质量分数为93.2%.
(8)试管2中反应生成的气体会使容器内压强增大,不利于使试管1中的液体进入试管2,图Ⅰ装置橡胶管A的作用是使试管1与试管2中气压相等,易于将稀盐酸从试管1加到试管2中,使稀盐酸的体积不引起测量误差;因二氧化碳能溶解于水,为了测定二氧化碳气体的体积准确,在装置中加入了二氧化碳不能溶于其中的食用油.
(9)A、二氧化碳气体受热体积膨胀,未冷却就读取量气管中液面刻度,测得气体的体积不准确,所以正确.
B、原装置中的空气与反应后剩余在装置中的气体体积相等,所以错误.
C、反应只消耗试管1中稀盐酸中的少许溶质,溶液的体积基本不变,所以错误.
故答案为:
(1)Mg(OH)2+CO2+2H2O═MgCO3?3H2O;
(2)玻璃棒;漏斗(或漏斗;玻璃棒);无白色沉淀出现或无明显现象等合理答案;
(3)不变;
(4)倾斜试管1,让稀盐酸从支管口流出进入试管2;气泡;
(5)调节量气管高度,使左右液面相平;
(6)100;
(7)解:设样品中4MgCO3?Mg(OH)2?4H2O的质量分数为x
4MgCO3?Mg(OH)2?4H2O~4CO2
466 176
2.5g×x (54-10)×10-3L×2.0g/L

x=93.2%
答:样品中4MgCO3?Mg(OH)2?4H2O的质量分数为93.2%.
(8)使试管1与试管2中气压相等,易于将稀盐酸从试管1加到试管2中,使稀盐酸的体积不引起测量误差;防止二氧化碳溶于水,影响实验;
(9)A.
点评:科学探究题是中考命题中一道亮丽的风景线,它往往从生活、生产实际出发,对身边常见物质或有趣的现象进行探究,既考查了学生综合运用知道的能力,又让学生体验科学探究的魅力,同时将探究结论应用在实际生活,体现了科学探究的意义和价值,这正是新课标中考的要求和方向.
(2)根据回答前一空;根据硫酸钠的性质回答后一空.
(3)根据液体能产生压强考虑回答.
(4)根据装置的结构回答.
(5)根据液柱造成的压强会影响气体体积回答.
(6)根据反应生成气体的体积判断量程.
(7)根据二氧化碳的密度计算出它的质量,再根据关系式 4MgCO3?Mg(OH)2?4H2O~4CO2计算MgCO3?Mg(OH)2?4H2O的质量,最后求质量分数.
(8)根据气压原理回答前一空;根据二氧化碳的溶解性回答后一空.
(9)A、根据气体热胀冷缩的性质判断.
B、根据原装置中的空气与反应后剩余在装置中的气体体积相等判断,
C、根据试管1中稀盐酸的体积变化不大判断.
解答:解:(1)根据信息“氢氧化镁悬浮液和二氧化碳在一定条件下生成MgCO3?3H2O沉淀”右得方程式为Mg(OH)2+CO2+2H2O═MgCO3?3H2O.
(2)过滤操作使用的玻璃仪器有:烧杯、玻璃棒、漏斗;由于硫酸钠能和可溶的钡盐反应生成白色沉淀,如沉淀没洗涤干净,则含有硫酸钠,滴加3滴氯化钡溶液,会生成白色沉淀,否则无沉淀生成.
(3)将水注入图Ⅱ中,弹簧夹夹紧橡胶管,提升量气管高度形成液差,如装置严密,气体压强不会减小,一段时间后,液差不变.
(4)将试管1中稀盐酸加到试管2中的具体操作方法是:倾斜试管1,让稀盐酸从支管口流出进入试管2.
(5)读取量气管内最终液面刻度前,需要进行的操作是调节量气管高度,使左右液面相平,否则管中的液柱能产生压强,对管中的气体进行压缩或拉伸,影响气体的体积测定.
(6)反应生成气体的体积为54mL,50mL的量气管量程太小,150mL的量气管不精确,所以选择100mL的量气管.
(7)解:设样品中4MgCO3?Mg(OH)2?4H2O的质量分数为x
4MgCO3?Mg(OH)2?4H2O~4CO2
466 176
2.5g×x (54-10)×10-3L×2.0g/L

x=93.2%
答:样品中4MgCO3?Mg(OH)2?4H2O的质量分数为93.2%.
(8)试管2中反应生成的气体会使容器内压强增大,不利于使试管1中的液体进入试管2,图Ⅰ装置橡胶管A的作用是使试管1与试管2中气压相等,易于将稀盐酸从试管1加到试管2中,使稀盐酸的体积不引起测量误差;因二氧化碳能溶解于水,为了测定二氧化碳气体的体积准确,在装置中加入了二氧化碳不能溶于其中的食用油.
(9)A、二氧化碳气体受热体积膨胀,未冷却就读取量气管中液面刻度,测得气体的体积不准确,所以正确.
B、原装置中的空气与反应后剩余在装置中的气体体积相等,所以错误.
C、反应只消耗试管1中稀盐酸中的少许溶质,溶液的体积基本不变,所以错误.
故答案为:
(1)Mg(OH)2+CO2+2H2O═MgCO3?3H2O;
(2)玻璃棒;漏斗(或漏斗;玻璃棒);无白色沉淀出现或无明显现象等合理答案;
(3)不变;
(4)倾斜试管1,让稀盐酸从支管口流出进入试管2;气泡;
(5)调节量气管高度,使左右液面相平;
(6)100;
(7)解:设样品中4MgCO3?Mg(OH)2?4H2O的质量分数为x
4MgCO3?Mg(OH)2?4H2O~4CO2
466 176
2.5g×x (54-10)×10-3L×2.0g/L

x=93.2%
答:样品中4MgCO3?Mg(OH)2?4H2O的质量分数为93.2%.
(8)使试管1与试管2中气压相等,易于将稀盐酸从试管1加到试管2中,使稀盐酸的体积不引起测量误差;防止二氧化碳溶于水,影响实验;
(9)A.
点评:科学探究题是中考命题中一道亮丽的风景线,它往往从生活、生产实际出发,对身边常见物质或有趣的现象进行探究,既考查了学生综合运用知道的能力,又让学生体验科学探究的魅力,同时将探究结论应用在实际生活,体现了科学探究的意义和价值,这正是新课标中考的要求和方向.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 轻质碳酸镁(化学式为4MgCO3?Mg(OH)2?4H2O)是制取氧化镁、颜料、油漆、日用化妆品的工业原料.
轻质碳酸镁(化学式为4MgCO3?Mg(OH)2?4H2O)是制取氧化镁、颜料、油漆、日用化妆品的工业原料.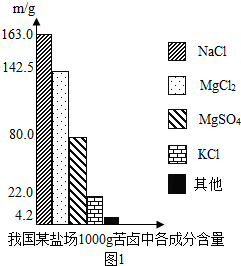
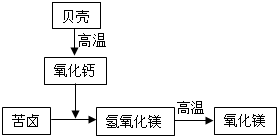
 4MgCO3?Mg(OH)2?4H2O+CO2↑+10H2O.
4MgCO3?Mg(OH)2?4H2O+CO2↑+10H2O.
 4MgCO3?Mg(OH)2?4H2O+CO2↑+10H2O.
4MgCO3?Mg(OH)2?4H2O+CO2↑+10H2O.