��Ŀ����
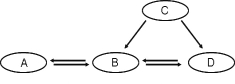
����Ŀ��(8��)ij��ѧ��ȤС�������µ�������(�¶�Ϊ20��)��Ϊ�˲ⶨH2SO4��NaOH�����кͷ�Ӧʱ�ų���������������ͼ��С�ձ��м���8mL������������Ϊ10%��NaOH��Һ(�ܶ�1 g/mL)��������3�η�̪���������¶ȣ���ȡ������ϡ����(�ܶ�1.12g/mL)���������¶Ⱥ��������������뵽С�ձ��У��ӱ��û��β���������������ձ�����Һ�¶ȵı仯�����ϡ�������֮���ϵ������ͼ��ʾ��

��1��������5 mLϡ����ʱ����Һ�е������� (��д���ʻ�ѧʽ)��
��2��������ԼΪ mLϡ����ʱ���ձ�����Һ���¶ȴﵽ��ߡ���ʱ�ձ�����Һ���¶�ԼΪ(��д����) �棬�ձ�����Һ��ɫ ��
��3��������ϡ������������10mLʱ����Һ�¶��½���ԭ���� ��
��4������Һ�¶��������ʱ����ʱ��Һ���������������Ƕ���?(д��������̣���3��)
���𰸡���1��Na2SO4��NaOH ��2��10mL 38��39 ��ɫ
��3��������ϡ��������ȴ������ɢ�� ��4��7.4��
��������
�����������1��H2SO4��NaOH�����кͷ�Ӧʱ�ų�����������������ͼ��֪��������10 mLϡ����ʱ����Һ���¶���ߣ���ʾ����ǡ����ȫ��Ӧ����������5 mLϡ����ʱ��NaOH�������ʴ�ʱ��Һ�е�������������Na2SO4�����й�����NaOH
��2����ͼ��������ԼΪ10mLϡ����ʱ���ձ�����Һ���¶ȴﵽ���������ԭ�¶�Ϊ20������Ӧ����ʹ�¶����ߴ�Լ18~19��������ʱ�ձ�����Һ���¶�ԼΪ38��39�����ڴ�ʱ����ǡ����ȫ��Ӧ����Һ�����ԣ����ձ�����Һ��ɫΪ��ɫ
��3��������ϡ������������10mLʱ����Һ�¶��½���ԭ������������ϡ��������ȴ������ɢ��
��4�����ݻ�ѧ����ʽ��2NaOH+H2SO4==Na2SO4+2H2O ��NaOH��Na2SO4��������ϵ�����������Na2SO4������
�⣺������Na2SO4������Ϊx
2NaOH+H2SO4==Na2SO4+2H2O
142
8mL��1g/mL��10% x
80��142=8mL��1g/mL��10%��x
x=1.42g
��Һ������=8mL��1g/mL+10mL��1.12g/mL=19.2g
��Һ��������������=1.42g/19.2g��100%=7.4%
����Һ��������������Ϊ7.4%