题目内容
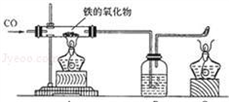
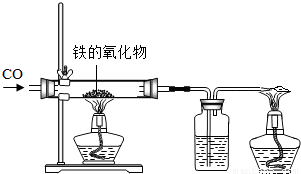
(1)小红用下图装置进行CO还原铁的某种氧化物实验,她先称量硬质玻璃管的质量为66.7g,往硬质玻璃管内放入该铁的氧化物后,称得铁的氧化物和硬质玻璃管的总质量是81.2g.然后通入CO并加热,使铁的氧化物与足量的CO充分反应,冷却后称得硬质玻璃管和管内残留固体的总质量是77.2g.由此推断,该氧化物的化学式为______;实验完毕称得洗气瓶的质量增加了______g.(2)某实验研究小组将6.5g由H2、O2、CO组成的混合气体置于密闭容器中点火爆炸.冷却至室温,干燥后测得气体质量为4.7g;再通入足量的苛性钠溶液,干燥后测得剩余气体质量为0.3g,经检验,这0.3g气体是氧气.求原混和气体中H2、O2、CO的质量各是多少?
【答案】分析:(1)根据质量守恒定律知:反应后玻璃管和管内固体的总质量去掉玻璃管的质量就是生成铁的质量,也是氧化物中铁元素的质量,反应前玻璃管和氧化物的总质量去掉玻璃管的质量就是氧化物的质量,再去掉铁元素的质量,就是氧化物中氧元素的质量,由氧化物中铁元素和氧元素的质量可以计算出氧化物中铁、氧元素的原子个数比,从而得到氧化物的化学式;根据氧化铁的质量,据化学方程式算的二氧化碳的质量,即为洗气瓶的质量增加量.
(2)根据题意获得反应生成的CO2质量以及生成H2O的质量,然后根据化学方程式计算即可.
解答:解:(1)氧化物中铁元素的质量:77.2g-66.7g=10.5g,铁的氧化物的质量:81.2g-66.7g=14.5g 铁的氧化物中氧元素的质量14.5g-10.5g=4.0g,氧化物中铁、氧元素的原子个数比为: =
= ,即氧化物的化学式为Fe3O4.
,即氧化物的化学式为Fe3O4.
设:生成二氧化碳的质量为x
4CO+Fe3O4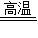 3Fe+4CO2
3Fe+4CO2
232 176
14.5g x
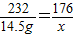 x=11g
x=11g
答:生成二氧化碳的质量为11g.
(2)解:反应生成的CO2质量为:4.7g-0.3g=4.4g,生成H2O的质量为:6.5g-4.7g=1.8g,
设:原混合气体中含CO的质量为X,含H2的质量为Y,分别与质量为m、n的O2反应
2CO+O2 2CO2
2CO2
56 32 88
X m 4.4g
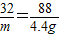 m=1.6g
m=1.6g
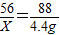 X=2.8g
X=2.8g
2H2+O2 2H2O
2H2O
4 32 36
Y n 1.8g
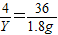 Y=0.2g
Y=0.2g
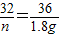 n=1.6g
n=1.6g
则原混合气体中含O2的质量为:0.3g+1.6g+1.6g=3.5g (或:6.5g-2.8g-0.2g=3.5g).
答:原混和气体中H2、O2、CO的质量各是0.2g、3.5g、2.8g.
点评:本题主要考查质量守恒定律和有关化学方程式的计算,要求学生会从题目已知信息中挖掘出暗藏的已知条件,并具备分析和解决问题的能力,难度较大,是一道综合实验和计算为一体的题目.
(2)根据题意获得反应生成的CO2质量以及生成H2O的质量,然后根据化学方程式计算即可.
解答:解:(1)氧化物中铁元素的质量:77.2g-66.7g=10.5g,铁的氧化物的质量:81.2g-66.7g=14.5g 铁的氧化物中氧元素的质量14.5g-10.5g=4.0g,氧化物中铁、氧元素的原子个数比为:
 =
= ,即氧化物的化学式为Fe3O4.
,即氧化物的化学式为Fe3O4.设:生成二氧化碳的质量为x
4CO+Fe3O4
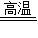 3Fe+4CO2
3Fe+4CO2232 176
14.5g x
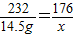 x=11g
x=11g答:生成二氧化碳的质量为11g.
(2)解:反应生成的CO2质量为:4.7g-0.3g=4.4g,生成H2O的质量为:6.5g-4.7g=1.8g,
设:原混合气体中含CO的质量为X,含H2的质量为Y,分别与质量为m、n的O2反应
2CO+O2
 2CO2
2CO256 32 88
X m 4.4g
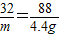 m=1.6g
m=1.6g 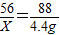 X=2.8g
X=2.8g2H2+O2
 2H2O
2H2O4 32 36
Y n 1.8g
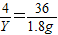 Y=0.2g
Y=0.2g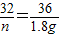 n=1.6g
n=1.6g 则原混合气体中含O2的质量为:0.3g+1.6g+1.6g=3.5g (或:6.5g-2.8g-0.2g=3.5g).
答:原混和气体中H2、O2、CO的质量各是0.2g、3.5g、2.8g.
点评:本题主要考查质量守恒定律和有关化学方程式的计算,要求学生会从题目已知信息中挖掘出暗藏的已知条件,并具备分析和解决问题的能力,难度较大,是一道综合实验和计算为一体的题目.

练习册系列答案
相关题目
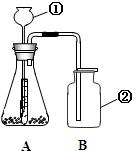 24、小红用下图装置制取二氧化碳,请完成下列问题:
24、小红用下图装置制取二氧化碳,请完成下列问题: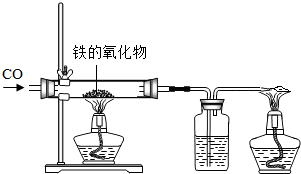 (1)小红用下图装置进行CO还原铁的某种氧化物实验,她先称量硬质玻璃管的质量为66.7g,往硬质玻璃管内放入该铁的氧化物后,称得铁的氧化物和硬质玻璃管的总质量是81.2g.然后通入CO并加热,使铁的氧化物与足量的CO充分反应,冷却后称得硬质玻璃管和管内残留固体的总质量是77.2g.由此推断,该氧化物的化学式为
(1)小红用下图装置进行CO还原铁的某种氧化物实验,她先称量硬质玻璃管的质量为66.7g,往硬质玻璃管内放入该铁的氧化物后,称得铁的氧化物和硬质玻璃管的总质量是81.2g.然后通入CO并加热,使铁的氧化物与足量的CO充分反应,冷却后称得硬质玻璃管和管内残留固体的总质量是77.2g.由此推断,该氧化物的化学式为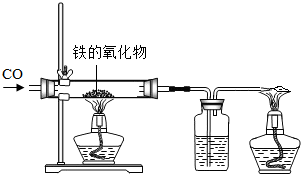 (1)小红用下图装置进行CO还原铁的某种氧化物实验,她先称量硬质玻璃管的质量为66.7g,往硬质玻璃管内放入该铁的氧化物后,称得铁的氧化物和硬质玻璃管的总质量是81.2g.然后通入CO并加热,使铁的氧化物与足量的CO充分反应,冷却后称得硬质玻璃管和管内残留固体的总质量是77.2g.由此推断,该氧化物的化学式为______;实验完毕称得洗气瓶的质量增加了______g.
(1)小红用下图装置进行CO还原铁的某种氧化物实验,她先称量硬质玻璃管的质量为66.7g,往硬质玻璃管内放入该铁的氧化物后,称得铁的氧化物和硬质玻璃管的总质量是81.2g.然后通入CO并加热,使铁的氧化物与足量的CO充分反应,冷却后称得硬质玻璃管和管内残留固体的总质量是77.2g.由此推断,该氧化物的化学式为______;实验完毕称得洗气瓶的质量增加了______g.