题目内容
(2007?青岛)小雪取刚降到地面的雨水并定时对其进行酸碱性强弱的测定,发现其pH均小于7且逐渐减小,直至稳定在pH=5.由此得出的结论是:雨水酸性逐渐
增强
增强
(填写“增强”、“减弱”或“不变”).该地区的西瓜适宜在pH为60~70的土壤环境中生长,此雨水对西瓜产量的影响是造成西瓜减产
造成西瓜减产
.煤等化石燃料燃烧产生的二氧化硫是形成酸雨的主要原因,为了减少或消除煤炭燃烧产生的二氧化硫,人们向煤炭中加入石灰石
石灰石
作为固硫剂制成型煤.分析:溶液的PH减小,酸性就增强,农作物一般适于在中性土壤中生长,如果酸性太强和碱性太强,都会造成减产;化石燃料燃烧产生的二氧化硫是形成酸雨的主要原因,因此就要让S不转化成二氧化硫排放出去.
解答:解:PH越小,酸性越强,雨水的pH均小于7且逐渐减小,直至稳定在pH=5,故雨水酸性逐渐 增强,雨水的PH小于西瓜最适宜的生长环境,故西瓜会减产.为了减少或消除煤炭燃烧产生的二氧化硫,人们向煤炭中加入石灰石作为固硫剂.
答案:增强、造成西瓜减产、石灰石
答案:增强、造成西瓜减产、石灰石
点评:溶液的PH越小,酸性就越强,农作物一般适宜在中性土壤中生长,过酸过碱都不利于作物生长.

练习册系列答案
相关题目
(2007?青岛)为了测定某品牌食用纯碱中碳酸钠的质量分数,某校化学研究性学习小组的探究过程如下:
[提出问题]样品中碳酸钠的质量分数是多少?
[知识准备]食用纯碱的主要成分是碳酸钠,另外还含有少量的氯化钠; 反应过程中不考虑水和氯化氢的挥发.
[设计方案]
(1)方案一:向一定量样品中加入过量澄清石灰水,根据反应生成碳酸钙的质量,先求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
(2)方案二:向一定量样品中加入足量的稀盐酸,根据反应生成二氧化碳的质量,先求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
[进行实验]
甲组同学:称取12.00g样品,加水配成溶液,在溶液中加入过量的澄清石灰水.过滤、洗涤、干燥,共得到白色沉淀10.00g.
乙组同学:称取12.00g样品,加入足量的稀盐酸直到反应停止,共收集到4.40g二氧化碳.
[解决问题]请你任选一组同学的实验结果,帮助他们计算出样品中碳酸钠的质量分数.(计算结果精确到0.1% )
[交流反思]
(1)甲组的小青同学认为,要求出碳酸钠的质量,也可以使用与盐酸和石灰水所属类别不同的其他物质______(填一种具体物质)的溶液与样品反应,通过测定相关物质的质量,进行有关计算即可.
(2)乙组的小雨同学认为,所用稀盐酸的溶质质量分数也可求出:取18.45g样品放入烧杯中,每次加入20g稀盐酸(不考虑水、氯化氢逸出)后用精密仪器称量,记录实验数据如下:
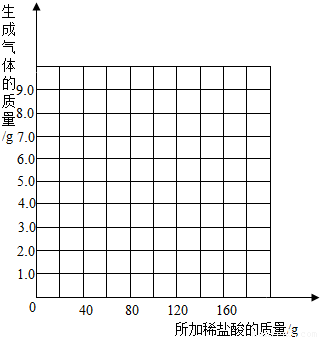
分析表中实验数据的变化规律,获取反应生成气体的质量,通过有关计算,即可求出稀盐酸的溶质质量分数.问题:请你在右边的坐标纸上绘制生成气体的质量与所加稀盐酸质量关系的曲线.
[提出问题]样品中碳酸钠的质量分数是多少?
[知识准备]食用纯碱的主要成分是碳酸钠,另外还含有少量的氯化钠; 反应过程中不考虑水和氯化氢的挥发.
[设计方案]
(1)方案一:向一定量样品中加入过量澄清石灰水,根据反应生成碳酸钙的质量,先求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
(2)方案二:向一定量样品中加入足量的稀盐酸,根据反应生成二氧化碳的质量,先求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
[进行实验]
甲组同学:称取12.00g样品,加水配成溶液,在溶液中加入过量的澄清石灰水.过滤、洗涤、干燥,共得到白色沉淀10.00g.
乙组同学:称取12.00g样品,加入足量的稀盐酸直到反应停止,共收集到4.40g二氧化碳.
[解决问题]请你任选一组同学的实验结果,帮助他们计算出样品中碳酸钠的质量分数.(计算结果精确到0.1% )
[交流反思]
(1)甲组的小青同学认为,要求出碳酸钠的质量,也可以使用与盐酸和石灰水所属类别不同的其他物质______(填一种具体物质)的溶液与样品反应,通过测定相关物质的质量,进行有关计算即可.
(2)乙组的小雨同学认为,所用稀盐酸的溶质质量分数也可求出:取18.45g样品放入烧杯中,每次加入20g稀盐酸(不考虑水、氯化氢逸出)后用精密仪器称量,记录实验数据如下:
| 加入稀盐酸次数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 烧杯及所称物质总质量/g | 78.90 | 97.80 | 116.70 | 135.60 | 155.05 | 175.05 | 195.05 |

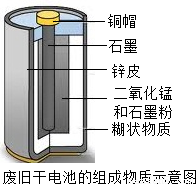
(2007?青岛)下面是某化学兴趣小组探究废旧干电池中白色糊状物成分的过程,
请帮助他们完成相应的报告.
[提出问题]白色糊状物是由什么物质组成的?
[资料]干电池的白色糊状物中含有铵根离子.
[猜想]可能含有OH-、CO32-、Cl-、SO42-中的一种或几种,白色糊状物可能是淀粉.
[设计方案]小亮首先认为不能存在的离子是______,因为铵根离子遇到该离子会生成氨气.
为了验证其他离子的存在情况,兴趣小组设计如下实验,请你完成以下实验报告.
[结论]干电池内白色糊状物中含有的盐类物质是______,在化肥中它属于______肥(填“氮”、“磷”、“钾”).
[反思]随意丢弃废旧干电池会造成环境污染,而废旧干电池中的许多物质可以回收利用,变废为宝,造福人类.
请帮助他们完成相应的报告.
[提出问题]白色糊状物是由什么物质组成的?
[资料]干电池的白色糊状物中含有铵根离子.
[猜想]可能含有OH-、CO32-、Cl-、SO42-中的一种或几种,白色糊状物可能是淀粉.
[设计方案]小亮首先认为不能存在的离子是______,因为铵根离子遇到该离子会生成氨气.
为了验证其他离子的存在情况,兴趣小组设计如下实验,请你完成以下实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| (1)取糊状物少量,加足量的水,搅拌后过滤.取少量滤液于试管中,滴加硝酸钡溶液. | ______ | 没有SO42-和CO32-存在 |
| (2)另取(1)所得滤液少量,滴加少量______溶液 | 产生白色沉淀 | 存在的离子是______ |
| (3)取白色糊状物,滴加少量______溶液 | 出现蓝色 | 有淀粉存在 |
[反思]随意丢弃废旧干电池会造成环境污染,而废旧干电池中的许多物质可以回收利用,变废为宝,造福人类.

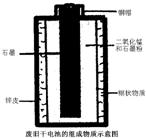 (2007?青岛)下面是某化学兴趣小组探究废旧干电池中白色糊状物成分的过程,
(2007?青岛)下面是某化学兴趣小组探究废旧干电池中白色糊状物成分的过程,