题目内容
根据氧化铁的化学式
Fe2O3计算(要求写出计算过程):(1)氧化铁中氧元素和铁元素的原子个数比和质量比.
(2)氧化铁中各元素的质量分数.
(3)80g氧化铁里含铁元素多少克.
(4)多少克氧化铁里含氧元素12g.
答案:
解析:
解析:
|
本题涉及了根据化学式的基本计算,计算中应注意,原子个数比就是化学式中元素符号右下角的数字比,元素质量比等于化学式中各原子的相对原子质量总和之比,元素的质量分数应按公式正确书写:元素的质量分数= |

练习册系列答案
相关题目
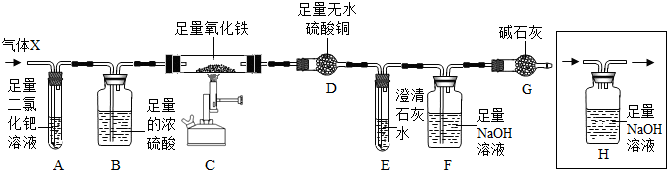
 在如图所示的有关物质转化关系中,各物质均是我们初中化学所学的物质.A是金属单质,C为红棕色固体粉末,B、D、K常温下都为气体,E、H都属于盐,F为能溶于水的碱.框图中有关反应的部分生成物没有标出.请根据框图中物质的转化关系填写下列空白:
在如图所示的有关物质转化关系中,各物质均是我们初中化学所学的物质.A是金属单质,C为红棕色固体粉末,B、D、K常温下都为气体,E、H都属于盐,F为能溶于水的碱.框图中有关反应的部分生成物没有标出.请根据框图中物质的转化关系填写下列空白: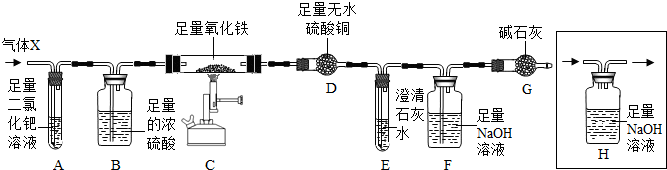
 8Fe+nCO2+2nH2O,其中n的值为______(填数字).
8Fe+nCO2+2nH2O,其中n的值为______(填数字).
 8Fe +nCO2+2nH2O,其中n的值为____________(填数字)。
8Fe +nCO2+2nH2O,其中n的值为____________(填数字)。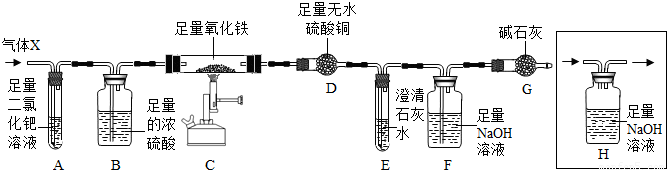
 8Fe+nCO2+2nH2O,其中n的值为______(填数字).
8Fe+nCO2+2nH2O,其中n的值为______(填数字).