题目内容
【题目】为了检验长期暴露在空气中的氢氧化钠固体是否变质,下列方法正确的( )
A. 用手接触,看是否有滑腻感 B. 滴加稀盐酸,看是否有气泡产生
C. 滴加酚酞,看是否变色 D. 滴加石灰水,看是否变浑浊
【答案】BD
【解析】A、药品不能用手直接触摸,因氢氧化钠有强腐蚀性.故A错误;B、滴加稀盐酸有气泡产生,生成气体,证明该物质中含有了碳酸根离子,也就是说明氢氧化钠变成了碳酸钠,故B正确;C、氢氧化钠和碳酸钠的溶液都显碱性,都能使酚酞变红,无法推断该氢氧化钠固体是否变质,故C错误;D、碳酸钠与石灰水反应产生白色沉淀,则滴加石灰水,石灰水变浑浊说明该固体中含有碳酸钠,则氢氧化钠已变质,故D正确;故选:B、D。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】某化学小组对一包干燥的红色粉末组成进行探究.请你参与并回答有关问题。
【教师提醒】它由Cu、Fe2O3二种固体中的一种或两种组成。
【提出猜想】红色粉末可能的组成有:①只有Cu;②只有_____________ ;③是Cu、Fe2O3的混合物。
【资料获悉】Cu在FeCl3溶液中发生的反应:2FeCl3+Cu═2FeCl2+CuCl2
Fe2O3与稀盐酸发生的反应:Fe2O3+6HCl═2FeCl3+3H2O
【实验探究】
(1)甲同学取少量红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解。甲同学认为可以排除猜想中的①和③,而乙同学认为只能排除猜想①,你认为__________ 的观点正确(填“甲”或“乙”)。
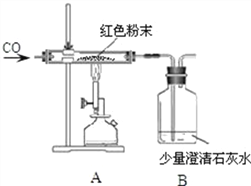
(2)丙同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按右图在通风橱中进行实验。开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表:
反应前 | 反应后 | |
Ⅰ组 | 玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
Ⅱ组 | 洗气瓶和所盛溶液的总质量为180.0g | 洗气瓶和瓶中物质的总质量为183.1g |
【交流讨论】
(1)在装置A中先通CO气体的作用是 ____________。
(2)应该选择_______组的实验数据计算来确定红色粉末的组成.最终计算结果表明:该红色粉末的组成是猜想中的第_______ 组(填序号)。
(3)实验中观察到A装置中的现象为_____________。【反思评价】丁同学指出:从环保角度,上图装置有严重不足之处.你认为应该如何改进?____________。