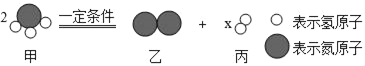题目内容
【题目】电视节目![]() 荒野求生
荒野求生![]() 中的生命吸管
中的生命吸管![]() 如图所示
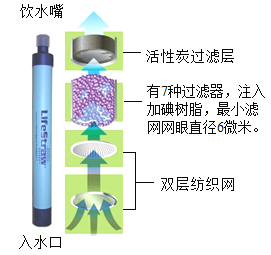
如图所示![]() 是一种将污水净化为饮用水的吸管装置,可以脱除色素、异味,但难以除去汞等金属离子。回答下列问题:
是一种将污水净化为饮用水的吸管装置,可以脱除色素、异味,但难以除去汞等金属离子。回答下列问题:
![]() 汞等金属离子危害人体健康的原因是:______。
汞等金属离子危害人体健康的原因是:______。
a导致坏死型肝硬化 b使人体蛋白质变性 c结合血红蛋白,抑制呼吸
![]() 生命吸管______
生命吸管______![]() “能”或“不能”
“能”或“不能”![]() 使硬水软化。家庭中使硬水软化一般采取______方法。
使硬水软化。家庭中使硬水软化一般采取______方法。
![]() 吸管中活性炭主要用来除去______。
吸管中活性炭主要用来除去______。
【答案】b 不能 加热煮沸 色素、异味等
【解析】
![]() 汞等金属离子能使蛋白质变性;故答案为:b;
汞等金属离子能使蛋白质变性;故答案为:b;
![]() 硬水中含有较多的镁离子、钙离子,生命吸管不能除去水中的镁离子、钙离子,不能使硬水软化。降低水的硬度的方法是:在生活中是加热煮沸,在实验室中是蒸馏;故答案为:不能;加热煮沸;
硬水中含有较多的镁离子、钙离子,生命吸管不能除去水中的镁离子、钙离子,不能使硬水软化。降低水的硬度的方法是:在生活中是加热煮沸,在实验室中是蒸馏;故答案为:不能;加热煮沸;
![]() 活性炭有吸附作用,可以吸附一些染料、色素、除去异味等;故答案为:色素、异味等;
活性炭有吸附作用,可以吸附一些染料、色素、除去异味等;故答案为:色素、异味等;

 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案【题目】化学学科实践活动课上,老师拿来一包粉末。它是由长期放置在空气中的铁粉和久置的碱石灰干燥剂混合而成,让同学们设计实验进行探究。
(提出问题)固体样品的成分是什么?
(查阅资料)(1)碱石灰干燥剂是CaO和NaOH的混合物。(2)CaCl2溶液显中性。
(猜想与假设)固体样品中可能含有 Fe、Fe2O3、CaO、NaOH、Ca(OH)2、Na2CO3和_____等七种物质。
(进行实验)
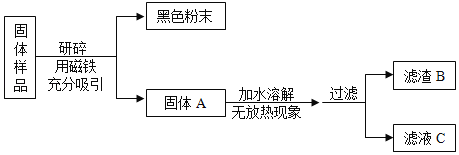
甲组同学对滤渣B的成分进行探究,记录如下:
实验操作 | 实验现象 | 实验结论及化学方程式 |
取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中 | ①_______________ ②_______________ | 结论:滤渣B中有 Fe2O3,CaCO3。 实验操作中Fe2O3与稀盐酸反应的化学方程式为:____________________ |
乙组同学对滤液C的成分进行探究,记录如下:
实验操作 | 实验现象 | 实验结论及化学方程式 |
取少量滤液C于试管中,加入过量CaCl2溶液,静置,向上层清液中滴加无色酚酞试液,振荡 | ①有白色沉淀生成 ②酚酞试液由无色变成红色 | 滤液C中有__________; 滤液C中的物质与CaCl2反应的化学方程式是_________________ |
(解释与结论)(1)乙组同学实验中加入过量CaCl2溶液的目的是________________________
(2)通过以上实验探究,该固体样品中能确定一定含有的成分是___________________。
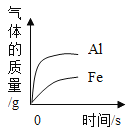
【题目】密闭容器内有M、N、P、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表,下列说法不正确的是( )
物质 | M | N | P | Q |
反应前质量/g | 19.7 | 8.7 | 31.6 | 0.4 |
反应后质量/g | 待测 | 17.4 | 19.7 | 3.6 |
A. 反应后密闭容器中M的质量为![]()
B. 该反应一定是化合反应
C. 物质P一定是化合物
D. 反应生成的N与Q的质量之比为87:32