��Ŀ����
����Ŀ��Ϊ��֤�����غ㶨�ɣ���������þ���ڿ�����ȼ�յ�ʵ�顣��ȼǰ���Ƚ�þ����_____��ĥ����������_____�����������ƣ��г�þ����ȼ���۲쵽�������Ǿ���ȼ�ա�_____�����ȡ�ð�����̡����ɰ�ɫ���塣���ȼ�պ���ʯ������ʣ����������С�ڷ�Ӧǰþ����������ԭ�������_____��ijͬѧ�����ֲ�������������ɫ���塣
���������ϣ�þ���뵪����Ӧ���ɵ���þ���壨Mg3N2�����仯ѧ����ʽ��_____��
����˼�뽻����������N2�ĺ���Զ����O2�ĺ�������þ���ڿ�����ȼ�����ɵ�����þȴԶ���ڵ���þ��ԭ����_____��
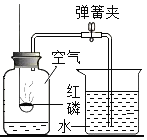
����չ��Ǩ�ƣ���������������������ʵ���У����װ�����������ã���������þƬ����Ӧֹͣ����ȴ�����£���ֹˮ�У����ּ���ƿ��Һ��_____ ������ڡ��������ڡ����ڡ��� ����ƿ�ݻ���![]() ��
��
���𰸡�ɰֽ ����ǯ ����ҫ�۵İ� ���ɵ�����þ������ɢ�������� 3Mg+N2![]() Mg3N2 ��ͬ������þ������������Ӧ ����
Mg3N2 ��ͬ������þ������������Ӧ ����
��������
þ���뵪����Ӧ���ɻ�ɫ�ĵ���þ���壬þ��������ȼ����������þ��
��ȼǰ���Ƚ�þ����ɰֽ��ĥ��������������ǯ�г�þ����ȼ���۲쵽�������Ǿ���ȼ�ա�����ҫ�۵İ⡢���ȡ��ܳ����̡����ɰ�ɫ���塣���ȼ�պ���ʯ������ʣ����������С�ڷ�Ӧǰþ����������ԭ����������ɵ�����þ������ɢ�������С�
[��������]þ���뵪����Ӧ���ɻ�ɫ�ĵ���þ���壨Mg3N2����Ӧ�Ļ�ѧ����ʽ�ǣ�3Mg+N2![]() Mg3N2��
Mg3N2��
[��˼�뽻��]������N2�ĺ���Զ����O2�ĺ�������þ���ڿ�����ȼ�����ɵ�����þȴԶ���ڵ���þ��ԭ������ͬ������þ������������Ӧ��
[��չ��Ǩ��]��������������������ʵ���У����װ�����������ã���������þƬ����Ӧֹͣ����ȴ�����£���ֹˮ�У���������Լռ��������������֮һ��þȼ�����������͵��������ս��뼯��ƿ�е�ˮ��������ڼ���ƿ�ݻ������֮һ����˷��ּ���ƿ��Һ����ڼ���ƿ�Ŀ̶ȡ�