题目内容
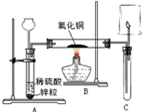 如图所示是实验室制取氢气并用氢气还原氧化铜的装置,根据图回答下列问题:
如图所示是实验室制取氢气并用氢气还原氧化铜的装置,根据图回答下列问题:(1)稀硫酸是由
长颈漏斗
长颈漏斗
加入,锌粒是从试管口
试管口
加入.加入的顺序是:先加锌粒
锌粒
后加酸;加入锌粒的具体操作是试管倾斜,用镊子夹取锌粒放在试管口,使试管慢慢竖起,将锌粒滑落试管底部
试管倾斜,用镊子夹取锌粒放在试管口,使试管慢慢竖起,将锌粒滑落试管底部
.(2)有关的化学方程式是
Zn+H2SO4═ZnSO4+H2↑
Zn+H2SO4═ZnSO4+H2↑
.(3)为使导管口的气体更容易点燃,试管C内盛放的液体通常是
浓硫酸
浓硫酸
.分析:根据已有的知识进行分析,加入药品的顺序是先固后液,根据颗粒状固体的加入方法进行解答,锌与稀硫酸反应生成硫酸锌和氢气,浓硫酸具有吸水性.
解答:解:(1)稀硫酸是由长颈漏斗加入,锌粒是从试管口加入.加入的顺序是先固后液,故先加锌粒后加酸,加入锌粒的具体操作是:试管倾斜,用镊子夹取锌粒放在试管口,使试管慢慢竖起,将锌粒滑落试管底部,故填:长颈漏斗,试管口,锌粒,试管倾斜,用镊子夹取锌粒放在试管口,使试管慢慢竖起,将锌粒滑落试管底部;
(2)锌与稀硫酸反应生成硫酸锌和氢气,故填:Zn+H2SO4═ZnSO4+H2↑;
(3)浓硫酸具有吸水性,能将氢气中混有的水分除去从而使氢气易于燃烧,故填:浓硫酸.
(2)锌与稀硫酸反应生成硫酸锌和氢气,故填:Zn+H2SO4═ZnSO4+H2↑;
(3)浓硫酸具有吸水性,能将氢气中混有的水分除去从而使氢气易于燃烧,故填:浓硫酸.
点评:本题考查了氢气的实验室制取,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目

 如图所示是实验室制取CO2的装置图,根据图回答下列问题.
如图所示是实验室制取CO2的装置图,根据图回答下列问题.