题目内容
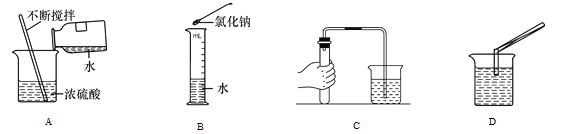
【题目】现提供下列装置:
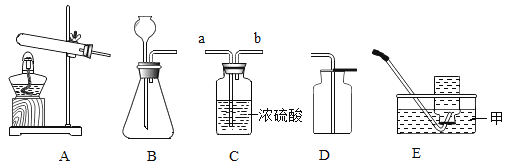
(1)上图E装置中,甲仪器的名称是___________。
(2)实验室用过氧化氢溶液和二氧化锰混合制O2发生装置可选用 _______(填装置序号),写出反应的化学方程式_____,用装置C干燥O2,气体由导管______端(填“a”或“b”)进入。
(3)英国化学家布莱克是第一个“捕捉”到CO2的人,实验室制备CO2的化学方程式为______;1774年德国化学家贝格曼将CO2通入紫色石蕊试液中,发现试液由紫色变为红色,此反应的化学方程式为_______。
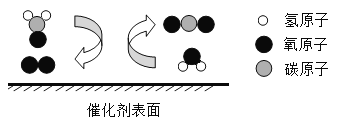
(4)如下装置用于一氧化碳还原氧化铁的实验,该装置集合了主反应的发生、产物检验和尾气处理于一体。
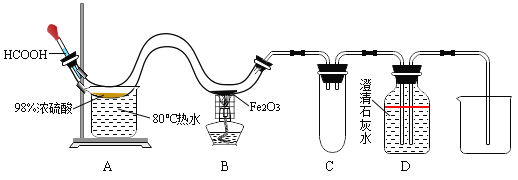
实验步骤如下:
步骤1:检查装置气密性。
步骤2:对W形管前端的浓硫酸进行80℃水浴加热。取下滴管,吸取甲酸(HCOOH)后连接于装置中,轻轻挤压滴管,将甲酸逐滴滴加到浓硫酸中。甲酸在浓硫酸的催化下反应生成一氧化碳和一种常见的液体。当D中集气瓶内液面下降到标记位置时,点燃B处酒精灯。
步骤3:当看到B中红棕色粉末全部变黑且装置D中出现相应的现象时,继续加热2-3分钟,而后熄灭酒精灯。
步骤4:检验B中得到的产物是铁。
步骤5:实验结束后,取下集气瓶,拿到安全之处,拔掉双孔塞,立即点燃尾气。
①步骤2中,当D中集气瓶内液面下降到标记位置时才点燃B处酒精灯,这样操作的原因是_________。
②实验过程中,装置B处(指W形管的后端内)发生反应的化学方程式为_____,装置D中集气瓶内的现象是_______。
③装置C的作用是_________。
【答案】水槽 B 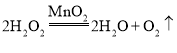 a CaCO3+2HCl=CaCl2+H2O+CO2↑ H2O+CO2=H2CO3 为了排尽装置内原有的空气,防止加热时发生爆炸
a CaCO3+2HCl=CaCl2+H2O+CO2↑ H2O+CO2=H2CO3 为了排尽装置内原有的空气,防止加热时发生爆炸 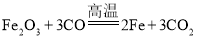 澄清石灰水变浑浊且集气瓶中液面下降 防止倒吸
澄清石灰水变浑浊且集气瓶中液面下降 防止倒吸
【解析】
(1)E装置中,甲仪器的名称是水槽;
(2)实验室用过氧化氢溶液和二氧化锰混合制O2,应选用固液常温发生装置,所以选用B,该反应的化学方程式为: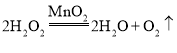 ,为了使混合气体与干燥剂充分接触,用装置C干燥O2,气体由导管a进入;
,为了使混合气体与干燥剂充分接触,用装置C干燥O2,气体由导管a进入;
(3)实验室采用石灰石和稀盐酸反应制备CO2,化学方程式为:![]() ,将CO2通入紫色石蕊试液中,发现试液由紫色变为红色,说明CO2和水反应生成了酸性物质碳酸,化学方程式为:
,将CO2通入紫色石蕊试液中,发现试液由紫色变为红色,说明CO2和水反应生成了酸性物质碳酸,化学方程式为:![]() ;
;
(4)①步骤2中,当D中集气瓶内液面下降到标记位置时才点燃B处酒精灯,这样操作是为了排尽装置内原有的空气,防止加热时发生爆炸;
②实验过程中,装置B处红棕色粉末全部变黑,说明氧化铁和一氧化碳反应生成了铁和二氧化碳,化学方程式为: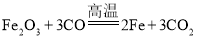 ,生成的二氧化碳使装置D中集气瓶内澄清石灰水变浑浊,当二氧化碳过量时集气瓶中液面下降;
,生成的二氧化碳使装置D中集气瓶内澄清石灰水变浑浊,当二氧化碳过量时集气瓶中液面下降;
③装置C的作用是防止倒吸。

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案【题目】皮蛋又称松花蛋,因其风味独特,深受人们喜爱。某兴趣小组在市场上获得了少许腌制皮蛋的原料。拿到实验室进行实验。将该固体混合物放于烧杯中,缓慢加入足量的蒸馏水,充分溶解后过滤,得到白色沉淀A和无色澄清滤液B。
【提出问题】![]() 白色沉淀A是什么?
白色沉淀A是什么?
(2)无色滤液B中的溶质有哪些?
【查阅资料】腌制皮蛋的原料配方是少量NaCl、CaO和过量![]() 的固体混合物。
的固体混合物。
【理论推理】![]() 白色沉淀A是
白色沉淀A是![]() ,请写出生成该沉淀的化学方程式______。
,请写出生成该沉淀的化学方程式______。
![]() 滤液B中含有
滤液B中含有![]() 、NaOH、NaCl三种溶质。
、NaOH、NaCl三种溶质。
【实验验证】为证明滤液B中存在的三种溶质,同学们进行了如下实验。
步骤 | 实验操作 | 实验现象 | 实验结论 |
I | 取少量滤液B于试管中,加入过量的 | ______ | 滤液B中含有 |
II | 取少量步骤I中所得滤液于试管中,加入酚酞溶液 | ______ | |
III | 另取少量步骤I中所得滤液于试管中,先加入足量的稀硝酸,再加入 ______ 溶液 | 产生白色沉淀 |
【拓展提升】
![]() 向步骤I中加入过量
向步骤I中加入过量![]() 溶液的目的是______。
溶液的目的是______。
![]() 小妮同学认为若将步骤I中的
小妮同学认为若将步骤I中的![]() 溶液换为
溶液换为![]() 溶液,进行以上实验,最终也能证明滤液B中存在的三种溶质。你认为是否合理______
溶液,进行以上实验,最终也能证明滤液B中存在的三种溶质。你认为是否合理______![]() 填“合理”或“不合理”
填“合理”或“不合理”![]() 。
。
![]() 小轩同学认为向滤液B中先加入酚酞溶液,后加入过量的
小轩同学认为向滤液B中先加入酚酞溶液,后加入过量的![]() 溶液,也能得出滤液B的溶质中含有
溶液,也能得出滤液B的溶质中含有![]() 和NaOH的结论,你是否同意他的观点并说明理由______。
和NaOH的结论,你是否同意他的观点并说明理由______。