题目内容
【题目】在一定质量的氯酸钾中加入15.8g高锰酸钾,充分混合后加热至完全反应,共制得氧气6.4g,
(1)根据化学方程式计算,15.8g高锰酸钾完全反应,生成氧气的质量。
(2)制得氧气中的氧元素占原混合物中氧元素的质量分数(计算结果保留到01.%)。
【答案】(1)1.6g (2)57.1%
【解析】
(1)根据高锰酸钾的质量结合化学方程式计算;(2)根据反应中氯酸钾中氧元素全部转化为氧气,高锰酸钾中中氧元素部分转化为氧气分析。
解:(1)设生成氧气的质量为x;
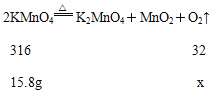
316/32=15.8g/x
x=1.6g
(2)高锰酸钾中氧元素的质量:15.8g×(64/158)=6.4g;
原混合物中氧元素的质量:(6.4g-1.6g)+6.4g=11.2g;
制得氧气中的氧元素占原混合物中氧元素的质量分数6.4g/11.2g×100%=57.1%
答: (1)生成氧气的质量为1.6g。
(2)制得氧气中的氧元素占原混合物中氧元素的质量分数为57.1%。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目