题目内容
向AgNO3和Cu(NO3)2混合溶液中加入一定量的锌粉,充分反应后再加入稀盐酸无明显现象.下列说法正确的是
A.一定有锌粉剩余 B.所得溶液中一定有Cu2+、Ag+ C.一定有银粉生成 D.
C
C
A.一定有锌粉剩余 B.所得溶液中一定有Cu2+、Ag+ C.一定有银粉生成 D.
锌粉没有剩余
锌粉没有剩余
.分析:根据金属活动性由强到弱的关系(Zn>Cu>Ag),锌首先置换硝酸银中的银,当硝酸银全部反应完后,锌可置换硝酸铜中的铜,充分反应后再加入稀盐酸无明显现象,说明了溶液中没有硝酸银,锌全部参加了反应,根据以上反应及现象,分析反应的发生情况,推断所得固体及溶液中的离子.
解答:解:由题意可知,向AgNO3和Cu(NO3)2混合溶液中加入一定量的锌粉,锌首先置换硝酸银中的银,当硝酸银全部反应完后,锌可置换硝酸铜中的铜.充分反应后再加入稀盐酸无明显现象,说明了溶液中没有硝酸银,锌没有剩余,铜不能确定.由此可知:
A、锌全部参加了反应,没有剩余,故A错误;
B、所得溶液中一定有Zn2+,Cu2+不能确定,故B错误;
C、溶液中没有硝酸银,一定有银粉生成,故C正确;
D、锌全部参加了反应,锌粉没有剩余,故D正确.
故选C,D增加锌粉没有剩余.
A、锌全部参加了反应,没有剩余,故A错误;
B、所得溶液中一定有Zn2+,Cu2+不能确定,故B错误;
C、溶液中没有硝酸银,一定有银粉生成,故C正确;
D、锌全部参加了反应,锌粉没有剩余,故D正确.
故选C,D增加锌粉没有剩余.
点评:本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目

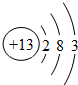 ,该原子在化学反应中易(填“得”或“失”)
,该原子在化学反应中易(填“得”或“失”)
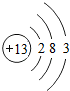 ,据此不能确定的是
,据此不能确定的是