题目内容
【题目】根据下列粒子结构示意图,回答问题。

(1)A、B、C、D所示粒子共表示______种元素(填数字)。
(2)D所示粒子在化学反应中容易_____电子(填“得到”或“失去”) 。
(3)若E中x=10 时,则该粒子属于____(填“原子”或“离子”)。
【答案】 3 得到 原子
【解析】在原子结构示意图中,小圆圈表示原子核,圆圈内的数字为质子数;弧线表示电子层,弧线上的数字为该层上的电子数。质子数决定原子的类别,A、B、C、D所示粒子共表示3种元素;原子的化学性质主要由最外层电子数决定,当最外层电子数小于4时,反应中易失去电子成为阳离子;当最外层电子数大于4时,反应中易得到电子成为阴离子;原子核外只有一个电子层且电子数为2,或者最外层电子数为8的结构为稳定结构,不易得失电子。D所示粒子在化学反应中容易得到电子;同一原子中,质子数=核外电子数=核电荷数=原子序数;在阳离子中:质子数>核外电子;在阴离子中:质子数<核外电子;若E中x=10 时,则该粒子属于原子。

 名校课堂系列答案
名校课堂系列答案【题目】安徽某水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水.)有关实验数据如表:
反应前 | 反应后 | ||
实验 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
180g | 12g | 187.6g | |
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为g.
(2)求该石灰石中碳酸钙的质量分数.
【题目】金属在生产、生活中有广泛的应用,认识金属的性质有利于更好地利用金属。
(1)用铜制作导线是利用铜的__________性。铁与硫酸铜溶液反应的化学方程式是_____________。
(2)铸造硬币用到Fe、Cu、Ni(镍)等金属,已知Ni能够发生如下反应:Ni+H2SO4=NiSO4+H2↑ Fe+NiCl2=Ni+FeCl2 则Fe、Cu、Ni三种金属活动性由强到弱的顺序为__________(用元素符号表示)。
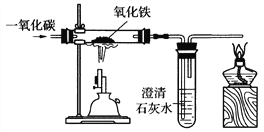
(3)炼铁的原理是利用一氧化碳与氧化铁反应,某同学设计的实验装置如下图:
①实验中玻璃管里的现象是_________,观察到试管里出现的现象是___________。
②该实验要先通CO后加热,目的是___________________。
(4)小强用一定量AgNO3和Cu(NO3)2的混合溶液进行如图实验,并对溶液A和固体B的成分进行分析和研究。
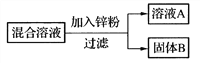
①溶液A中的溶质一定含有______________,可能含有_______________。
②通过以下实验可确定固体B的成分,请将下表填写完整。
实验步骤 | 现象 | 实验结论 |
取少量固体B,滴加_________ | 有气泡产生 | 固体B中含有Cu 、Ag和_____ |
【题目】某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象,硫酸中混有硫酸铜溶液时,产生氢气的速率更快.
【提出问题】是什么离子导致产生氢气的速率加快?
(1)【猜想假设】他们分别对这种意外现象作如下猜想:
甲同学:可能与铜离子有关;
乙同学:可能与硫酸根离子有关;
丙同学认为乙的猜想不科学,理由是 .
(2)【实验证明】用A、B两组仪器进行实验: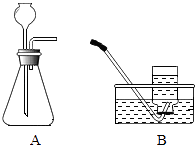
步骤一:检查装置气密性.检查图A所示装置气密性,你采用的方法是 .
步骤二:量取2份质量分数为20%的稀硫酸各20mL,第一份加入质量分数为10%的稀硫酸铜溶液1mL,第二份加入质量分数为10%的硫酸锌溶液1mL,称取2份形状相同锌粒各1g,分别与以上溶液反应,反应装置如图A所示,用此装置实验时,长颈漏斗下端要插入液面以下,目的是 .
实验三:用B收集气体,分别记录收集一瓶气体(集气瓶规格均为125mL)所需的时间(如表),什么时间开始收集气体? .
编号 | 20%的硫酸各20ml | 锌粒 | 收集1瓶氢气所需的时间 |
① | 加入质量分数为10%的硫酸铜溶液1ml | 1g | 2分10秒 |
② | 加入质量分数为10%的硫酸锌溶液1ml | 1g | 3分01秒 |
锌与硫酸反应的化学方程式是 .
(3)【得出结论】硫酸中混有硫酸铜溶液时,产生氢气的速率加快与有关,实验②中加入质量分数为10%的硫酸锌溶液1ml的作用是 .
(4)【反思质疑】丁同学认为:锌与混有硫酸铜的硫酸溶液反应时,产生氢气的速率较快可能与铜单质有关,他质疑的理由是 .
(5)【继续探究】请你设计一个实验方案验证丁同学的观点是否正确.
编号 | 实验步骤 | 实验现象比较 | 实验结论 |
① | 取1g锌粒于锥形瓶中,加入20ml20%的稀硫酸 | 产生氢气的速率较快与铜单质有关 | |
② |