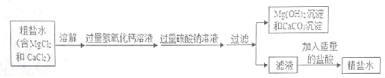
ЬтФПФкШн
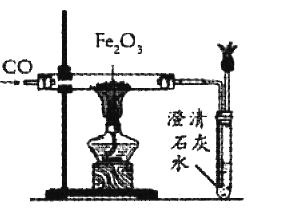
ЁОЬтФПЁПФГЬњПѓЗлЃЌжївЊГЩЗжЮЊЬњЕФбѕЛЏЮяЃЈFeXOyЃЉЃЌвЛбЇЩњРћгУЪЕбщзїНјвЛВНЗжЮіЃЌЙ§ГЬМАЪ§ОнШчЯТЁЃЃЈзЂЃКЬњПѓЗлжадгжЪВЛВЮгыЯТСаЙ§ГЬжаЕФЗДгІЃЉ
ЂёЃЎШЁ30gИУЬњПѓЗлдкCOЦјСїжаГфЗжМгШШЃЌНЋЗДгІКѓЕФЦјЬхгУЩеМюШмвКГфЗжЮќЪеЃЌЩеМюШмвКдіжи17.6g
ЂђЃЎНЋЩЯЪіМгШШКѓЕФЙЬЬхШЁГіКѓЃЌдйЯђЙЬЬхж№ЕЮМгШыЯЁСђЫсЃЌВтЕУВњЩњЦјЬхгыЕЮШыЯЁСђЫсЕФжЪСПЙиЯЕШчЭМЃК
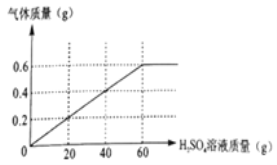
ЭЈЙ§МЦЫуЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉ30gЬњПѓЗлЫљКЌЬњЕФбѕЛЏЮяжаЃЌЬњдЊЫиЕФжЪСПЮЊ______gЃЌбѕдЊЫиЕФжЪСПЮЊ______gЁЃ
ЃЈ2ЃЉИУЬњЕФбѕЛЏЮяЛЏбЇЪНжаЃЌxЁЂyЕФзюМђећЪ§БШxЃКy=______ЁЃ
ЁОД№АИЁП16.8 6.4 3ЃК4
ЁОНтЮіЁП
ЃЈ1ЃЉЩшЬњЕФжЪСПЮЊx

НтЕУЃКm=16.8g
гЩжЪСПЪиКуЖЈТЩПЩжЊЃЌЬњЕФбѕЛЏЮяжабѕдЊЫиЕФжЪСПЮЊЃК17.6gЁС![]() ЁС
ЁС![]() =6.4g
=6.4g
ЃЈ2ЃЉгЩЩЯЪіМЦЫуПЩжЊЃК![]() НтЕУЃК
НтЕУЃК![]() ЁЃ
ЁЃ
Д№АИЃКЃЈ1ЃЉ16.8ЃЛ6.4ЃЛЃЈ2ЃЉ3ЃК4

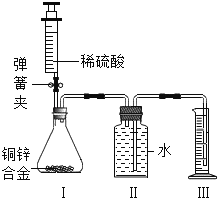
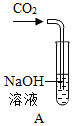
ЁОЬтФПЁПЖдБШЪЕбщЪЧЛЏбЇбаОПжаОГЃВЩгУЕФЗНЗЈЁЃЛЏбЇаЫШЄаЁзщЕФЭЌбЇЮЊбаОПCO2ЭЈШыNaOHШмвКЪЧЗёЗЂЩњСЫЗДгІ,ЩшМЦСЫЯТСаЪЕбщЁЃЧыКЭЛЏбЇаЫШЄаЁзщЕФЭЌбЇвЛЦ№ЬНОПВЂЛиД№ЮЪЬтЃК
ЃЈЩшМЦгыЪЕбщЃЉ
ЪЕбщ | ЪЕбщВНжшвЛ | ЪЕбщВНжшЖў | ЪЕбщ | ЪЕбщВНжшвЛ | ЪЕбщВНжшЖў |
ЪЕбщI |
|
| ЪЕбщII |
|
|
ЃЈЬНОПгыНсТлЃЉ
(1)ЪЕбщIжаВНжшвЛЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ____________________________ЃЌВНжшЖўВњЩњЕФЯжЯѓЪЧ________________ЁЃ
(2)ЪЕбщЂђжаВНжшЖўЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ____________________________ЁЃ
CaCl2ШмвКвВПЩвдгУ______(ЬюађКХ)ДњЬцДяЕНЪЕбщФПЕФЁЃ
AЯѕЫсБЕШмвК BТШЛЏМиШмвК
CЬМЫсМиШмвК DСђЫсФЦШмвК
(3)ЪЕбщНсЪјКѓ,гжгаЭЌбЇЬсГіПЩЯђЭЈШызуСПCO2ЕФNaOHШмвКжаЕЮМгЮоЩЋЗгЬЊ,ХаЖЯСНепЪЧЗёЗЂЩњЗДгІЁЃСЂТэБЛаЁзщЭЌбЇЗёЖЈ,двђЪЧ____________________________ЁЃ
ЃЈВщдФзЪСЯЃЉ
ЮяжЪ | ШмНтЖШЃЈsЃЉ/g |
NaOH | 17.3 |
Na2CO3 | ЃМ0.01 |
(4)ЭЌбЇУЧдкВщдФзЪСЯКѓгжЩшМЦСЫЪЕбщЂѓЃЌНЋCO2ЭЈШыNaOHЕФОЦОЋШмвКЃЌЕБЙлВьЕН____________ЕФЯжЯѓЃЌжЄУїСНепШЗЪЕЗЂЩњСЫЗДгІЁЃ