题目内容
请你参与下列探究:[问题情景]某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出.这一现象激发起同学们的探究欲望,生成的是什么气体?
[提出猜想]从元素守恒的角度,放出的气体可能是SO2、O2、H2.
[查阅资料]SO2易溶于水,它能与NaOH反应,生成Na2SO3.
[方案设计]依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,则检验方法是
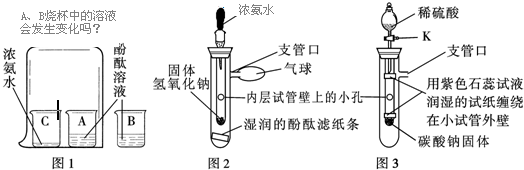
(2)乙同学认为是SO2,则只需将放出的气体通入盛有NaOH溶液的洗气瓶中,称量通气前后洗气瓶的质量.写出SO2与NaOH反应的化学方程式
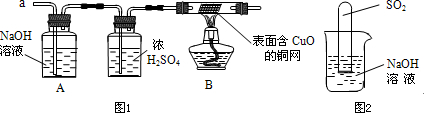
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体.
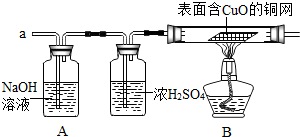
如果放出的是O2和H2,你认为方案中的安全隐患是
老师说:化学反应中,一种元素的化合价升高,肯定有元素的化合价降低,这是科学规律.丙同学根据老师这句话,说:“肯定不是
[实验探究]小组同学首先对装置A进行称量,再将收集到的气体从a通入,过一会儿点燃B处酒精灯;一段时间后,发现表面含CuO的铜网由黑色变为光亮的红色,B装置的尾部有水珠生成;停止通气,再次称量装置A,发现质量无增减.
结论:铁粉与硫酸铜溶液反应时,产生的气体是
[思维拓展](1)由上述实验可以推出,硫酸铜溶液中可能含有
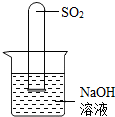
(2)不通过称量,如何判断SO2与NaOH溶液发生了反应呢?丁同学设计了如图所示的装置进行实验,发现试管内液面上升,就得出SO2与NaOH溶液发生反应的结论.其他同学认为这一方案不严谨,理由是
分析:[方案设计](1)验证是否为氧气,检验氧气的方法;
(2)根据氢氧化钠的性质,判断氢氧化钠与二氧化硫反应的反应物和生产物,正确书写化学方程式;
(3)可燃性气体不纯会爆炸.
[实验探究]因为“发现表面含CuO的铜网由黑色变为光亮的红色;停止通气,再次称量装置A,发现质量不变”,所以产生的气体为氢气;书写氢气还原氧化铜的化学方程式.
[思维拓展](1)因为加入金属铁有氢气生成,所以溶液中含有游离的氢离子存在,含氢离子的溶液呈酸性;
(2)二氧化硫不但与氢氧化钠溶液反应,还和水反应,利用对比实验进行检验.
(2)根据氢氧化钠的性质,判断氢氧化钠与二氧化硫反应的反应物和生产物,正确书写化学方程式;
(3)可燃性气体不纯会爆炸.
[实验探究]因为“发现表面含CuO的铜网由黑色变为光亮的红色;停止通气,再次称量装置A,发现质量不变”,所以产生的气体为氢气;书写氢气还原氧化铜的化学方程式.
[思维拓展](1)因为加入金属铁有氢气生成,所以溶液中含有游离的氢离子存在,含氢离子的溶液呈酸性;
(2)二氧化硫不但与氢氧化钠溶液反应,还和水反应,利用对比实验进行检验.
解答:解:
[方案设计](1)氧气的检验方法是:用带火星的木条,能够复燃说明是氧气;
(2)SO2与NaOH反应生成亚硫酸钠和水,反应的化学方程式为SO2+2NaOH=Na2SO3+H2O;
(3)如果放出的是O2和H2,可燃性气体氢气不纯点燃时会爆炸,实验时在B处易发生爆炸事故;
根据化学反应中,一种元素的化合价升高,肯定有元素的化合价降低,若生成气体含氧气,O元素化合价升高,则必定还含有H或S元素化合价降低所产生的氢气或二氧化硫气体,因此,所得气体肯定不能是氧气;
[实验探究]含CuO的铜网由黑色变为光亮的红色说明有还原性气体即氢气,氢气还原氧化铜的化学方程式CuO+H2
Cu+H2O;
[思维拓展]](1)因为有氢气生成,铁应该与酸反应产生氢气,所以要有游离的氢离子存在,则知硫酸铜溶液显酸性;
(2)为了更严谨,应将氢氧化钠溶液换成水,对比二氧化硫与水反应时液面上升的情况.
故答案为:
[方案设计](1)用带火星的木条试验,木条复燃则是氧气;
(2)SO2+2NaOH=Na2SO3+H2O;
(3)实验时在B处易发生爆炸事故;氧气;
[实验探究]H2;H2+CuO
Cu+H2O;
[思维拓展](1)酸性;(2)SO2易溶于水,也能使液面上升;将NaOH溶液换成水做对比实验.
[方案设计](1)氧气的检验方法是:用带火星的木条,能够复燃说明是氧气;
(2)SO2与NaOH反应生成亚硫酸钠和水,反应的化学方程式为SO2+2NaOH=Na2SO3+H2O;
(3)如果放出的是O2和H2,可燃性气体氢气不纯点燃时会爆炸,实验时在B处易发生爆炸事故;
根据化学反应中,一种元素的化合价升高,肯定有元素的化合价降低,若生成气体含氧气,O元素化合价升高,则必定还含有H或S元素化合价降低所产生的氢气或二氧化硫气体,因此,所得气体肯定不能是氧气;
[实验探究]含CuO的铜网由黑色变为光亮的红色说明有还原性气体即氢气,氢气还原氧化铜的化学方程式CuO+H2
| ||
[思维拓展]](1)因为有氢气生成,铁应该与酸反应产生氢气,所以要有游离的氢离子存在,则知硫酸铜溶液显酸性;
(2)为了更严谨,应将氢氧化钠溶液换成水,对比二氧化硫与水反应时液面上升的情况.
故答案为:
[方案设计](1)用带火星的木条试验,木条复燃则是氧气;
(2)SO2+2NaOH=Na2SO3+H2O;
(3)实验时在B处易发生爆炸事故;氧气;
[实验探究]H2;H2+CuO
| ||
[思维拓展](1)酸性;(2)SO2易溶于水,也能使液面上升;将NaOH溶液换成水做对比实验.
点评:本题主要考查化学实验的方案设计与评价,了解猜想和事实验证的方法及防范爆炸的措施,掌握氧气的检验方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目