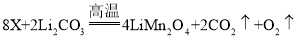题目内容
【题目】小明同学已经知道镁能与氧气反应,还想用金属镁设计实验验证金属的其它化学性质。
预测 | 预测的依据 | 验证预测的实验操作与预期现象 |
①能够与酸反应 | 锌能与稀硫酸反应产生氢气,镁比锌活泼。 | _____,则预测成立 |
②能够与盐反应 | _____ | 往装有2mLCuSO4溶液的试管中放入一根用砂纸打磨干净的镁条,观察到镁条表面有气泡,一段时间后,蓝色溶液变淡,试管底部有红色固体。 |
小明发现,镁条放入CuSO4溶液中,镁条表面有气泡产生,为什么呢?小明想,镁是不是能跟水发生反应呢?
于是,他将镁条放到盛有冷水(蒸馏水)的试管中,没有明显的现象,然后将试管放在酒精灯上加热,发现试管中有气泡产生。
(提出问题)加热时镁条与水发生反应吗?生成的物质是什么呢?
(猜想与假设)
(1)甲同学认为,加热时应该先将蒸馏水煮沸并迅速冷却,理由是_____。
(2)甲同学认为,加热时镁和水反应生成的气体是_____(选填a、H2或b、N2),不选择另一项的理由是_____。
(实验验证)乙同学向加热的试管中滴入酚酞溶液,溶液显红色。
(实验结论)
(3)镁在加热时与水发生反应,因为加热后溶液中生成了_____性物质。请根据分析写出二者反应的化学方程式_____,看来,关于镁与硫酸铜溶液的反应还是比较复杂的,小明决定接下来跟老师一起继续探究。
【答案】往装有2mL稀硫酸溶液的试管中放入一根用砂纸打磨干净的镁条,观察到镁条表面有气泡产生 铁能与硫酸铜溶液反应,镁比铁活泼 排除溶解在水中的气体 a、H2 反应物中不含有氮元素,不能生成氮气 碱 Mg+2H2O![]() Mg(OH)2+H2↑
Mg(OH)2+H2↑
【解析】
①锌可与反应生成氢气,因此设计实验,将镁放入硫酸中,观察是否有气泡,即可判断镁与酸能否可以反应;验证预测的实验操作与预期现象是:往装有2mL稀硫酸溶液的试管中放入一根用砂纸打磨干净的镁条,观察到镁条表面有气泡产生;
②镁与硫酸铜可以发生置换反应生成铜,因此需要在预测中,只要找到常见金属活动性比镁弱,但是强于铜,进行预测其可与硫酸铜反应,然后再对比镁与该金属的性质,即可完成实验预测;预测的依据是:铁能与硫酸铜溶液反应,镁比铁活泼;
(1)由于气体加热溶解度变小,因此为了避免水中溶解的气体影响实验结果,需要加热排除内部气体,避免影响实验;
(2)根据质量守恒定律,反应物含有可以生成气体的元素为水中的氢、氧元素,可以生成氢气或者氧气,而氧气可与金属反应,不能形成气泡,所以气体为氢气,反应物中不含有氮元素,因此生成物不能含有氮元素,也就不能生成氮气;
(3)加入酚酞变红,说明溶液显碱性;所以镁与水在加热时反应生成了氢气和氢氧化镁,反应的化学方程式为:Mg+2H2O![]() Mg(OH)2+H2↑。
Mg(OH)2+H2↑。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】我国自主设计的大型客机成功试飞,首艘国产航母正式下水,标志着我国的金属材料制造技术取得重大突破。根据所学知识回答下列问题:
金属 | A | B | C | D |
导电性(以100为标准) | 99 | 61 | 17 | 7.9 |
密度/ (g﹒cm-3) | 8.92 | 2.70 | 7.86 | 11.3 |
熔点/°C | 1083 | 660 | 1535 | 327 |
硬度(以10为标准) | 3 | 2.7 | 5 | 1.5 |
(1)常温下一些金属的物理性质数据如表。据此可知高压输电线最好选用金属_____________(填字母): C的合金通常可以做菜刀、锤子等。其合金的硬度_____________5(填“>”、“<”或“=”).
(2)铁矿石有多种,如赤铁矿(主要成分Fe2O3)和磁铁矿(主要成分Fe3O4)等,写出磁铁矿的主要成分与一氧化碳反应炼铁的化学方程式___________________________。
(3)铬(Cr)也是一种重要的金属元素,铬单质及其化合物应用广泛。重铬酸钾(K2Cr2O7)可用于测试酒驾,则重铬酸钾中铬元素的化合价为__________________。
(4)铬桶可以盛装AlCl3溶液,不能盛装稀硫酸,则金属活动性,Cr__________ Al(填“>” 或“<”)。根据上述信息,不能证明Zn和Cr的活动性强弱的试剂组是__________________。
a Zn、Cr和稀硫酸
b Cr、ZnSO4溶液
c Cu、ZnSO4溶液、CrSO4溶液
(5)Cr2(SO4)3为有毒的重金属盐,可用NaOH溶液将其转化为沉淀而除去,该转化的化学方程式为__________________。
【题目】氧化镁在医药等行业应用广泛。实验室以菱镁矿(主要成分为MgCO3,含少量FeCO3,其他杂质不溶于水和酸)为原料制备高纯氧化镁的实验流程如下:
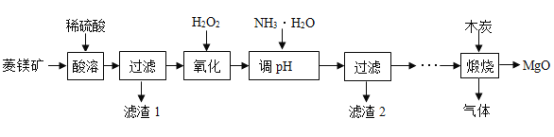
(1)为了提高“酸浸”的效果,可采取的措施有:适当升高温度、____________。MgCO3与稀硫酸反应的化学方程式为_________________。
(2)“氧化”过程中,将FeSO4全部转化为Fe2(SO4) 3,然后加氨水,调节溶液的PH范围为______________。(已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表)
对应离子 | Fe3+ | Fe2+ | Mg2+ |
开始沉淀时的pH | 2.7 | 7.9 | 9.4 |
完全沉淀时的pH | 3.7 | 9.6 | 11.4 |
(3)过滤后得到滤渣2和滤液,滤渣2是______(填化学式),此时滤液中的阳离子一定含有____________(填离子符号)。
(4)煅烧过程存在以下反应:![]() ;
;![]() ;
;![]()
已知:①硫在常温下是一种淡黄色固体,硫的熔点约为115.2°C,沸点约为444.7°C;②高锰酸钾溶液与SO2反应会褪色,且只吸收SO2,不吸收CO2;③碱溶液既吸收SO2,又吸收CO2。利用下图装置对煅烧产生的气体进行检验并收集。
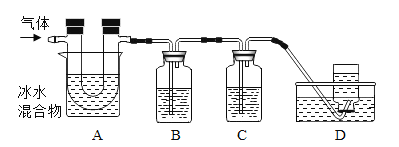
①集气瓶B中盛放的溶液是_______________(填字母),C中盛放的溶液是_____________(填字母)。
a Ca(OH)2溶液
b KMnO4溶液
c NaOH溶液
d BaCl2溶液
②装置D的作用是__________________________。