题目内容
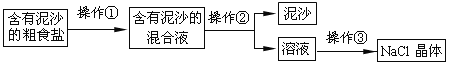
【题目】山西省是重要的煤化工基地,煤及其相关产品是转型发展的方向之一,以煤层气(主要成分是甲烷)、焦炭、水、空气为原料,可制得若干产品,部分生产过程如图:
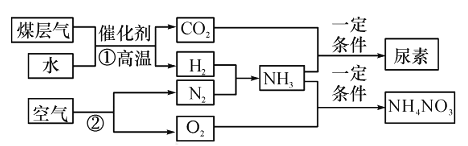
请回答下列问题:
(1)过程②是利用分离液态空气法进行分离的,该变化是_____(填“物理”或“化学”)变化.
(2)写出①所发生反应的化学方程式_____.
(3)下列说法正确的是_____.
a无机物可以转化成有机物
b氮气在工业上可用于制尿素、硝酸铵等氮肥
c生产过程使煤及其相关产品得到了综合利用
(4)尿素和NH4NO3都是氮肥,其中NH4NO3中氮元素与氧元素的质量比为_____,100gNH4NO3中氮元素的质量为_____g.
【答案】物理 CH4+2H2O![]() CO2+4H2 abc 7:12 35
CO2+4H2 abc 7:12 35
【解析】
(1)过程②是利用分离液态空气法进行分离的,是利用氧气和氮气的沸点不同,过程中无新物质生成,为物理变化.
(2)反应物为甲烷和水,反应条件为高温和催化剂,生成物为二氧化碳和请,配平时先假设甲烷的系数为1.则得到对应的化学方程式为:CH4+2H2O![]() CO2+4H2.
CO2+4H2.
(3)a.有题目给出的转化关系,无机物二氧化碳和氨气在一定条件下生成了有机物尿素,所以无机物可以转化成有机物.正确;
b.根据质量守恒定律和本题的转化关系都可以得知,氮气在工业上可用于制尿素、硝酸铵等氮肥.正确;
c.本题实现了煤及其相关产品的综合利用,所以生产过程使煤及其相关产品得到了综合利用的说法是正确的.正确.
故选:abc.
(4)NH4NO3中氮元素与氧元素的质量比为(14×2):(16×3)=7:12,100gNH4NO3中氮元素的质量为![]() .
.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示。同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究。

(提出问题)久置固体的成分是什么?
(查阅资料)铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
(猜想)久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。
(实验探究1)甲同学的方案:
实验操作 | 实验现象 | 实验结论 |
(1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红 | 固体中一定含有____和Ca(OH)2. |
(2)另取少量固体放于试管中,滴加足量的____ | 固体逐渐消失,有无色气体产生,得到浅绿色溶液 | 固体中一定含有Fe,一定不含Fe2O3 |
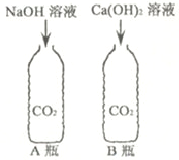
(3)将步骤(2)中产生的气体通入到澄清石灰水中 | ____ | 固体中一定含有CaCO3 |
(实验质疑)
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是_____。
(2)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是_____。
(实验探究2)
乙、丙同学设计如下实验方案继续验证:
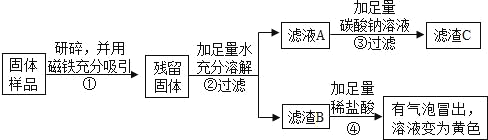
(1)③中反应的化学方程式是_____。
(2)乙、丙同学实验中能得出固体样品中一定还含有_____,仍有一种物质不能确定,该物质是_____。
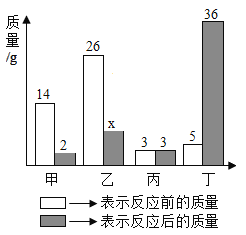
(3)乙、丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g。
(实验结论)综合上述实验及所给数据,久置固体的成分是_____。