题目内容
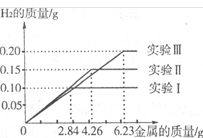
在今年全国两会期间,代表们所使用的石头纸、环保手提袋和购物袋,主要原料是具有环保意义的碳酸钙。为测定某石头纸中碳酸钙的含量,某同学称取10g碎纸样品放入烧杯中,将50g 盐酸分5次加入烧杯。实验数据见下表(假设纸张其他成分既不溶于水,也不与盐酸反应):
(1)10g样品与足量稀盐酸反应最多生成 g气体。
(2)计算样品中碳酸钙的质量分数。(写出计算过程)
| | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入稀盐酸的质量/g | 10 | 10 | 10 | 10 | 10 |
| 充分反应后烧杯及烧杯中物质总质量/g | 209.12 | 218.24 | 227.36 | 236.48 | 246.48 |
(2)计算样品中碳酸钙的质量分数。(写出计算过程)
(1)3.52g
(2)80%
(2)80%
试题分析:(1)由题意分析,根据质量守恒定律,可得前四次实验后碳酸钙恰好完全反应,且每次均放出二氧化碳0.88g;则10g样品与足量稀盐酸反应,最多生成二氧化碳的质量=0.88g×4=3.52g;
(2)[解]设:碳酸钙样品中碳酸钙的质量为x
CaCO3 + 2HCl ="==" CaCl2 + H2O + CO2↑
100 44
x 3.52g
x = 8g
样品中碳酸钙的质量分数=
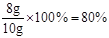
答:样品中碳酸钙的质量分数为80%
点评:根据质量守恒定律分析题中数据,得出二氧化碳的质量是解题的关键;根据化学方程式计算,要注意解题的步骤,设、写、找、列、解、答。

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案
相关题目