题目内容
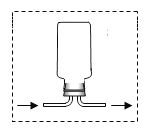
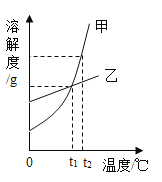
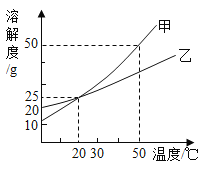
【题目】如图是甲,乙两种固体物质的溶解度曲线。20℃时,向150g水中可加入50g甲,充分搅拌后所得甲溶液的溶质质量分数为_______;50℃时.将甲、乙的饱和溶液恒温蒸发,若得到相同质量的甲、乙固体,需要蒸发掉水的质量关系为甲_________乙(填“大于”“小于”或“等于”)。20℃时,将125g甲的饱和溶液稀释至溶质质量分数为10%的甲溶液,需加水______g。
【答案】20% 小于 125
【解析】
20℃时,甲的溶解度是25g,150g水中可以溶解37.5g的甲物质,加入50g甲,不能完全溶解,充分搅拌后所得甲溶液的溶质质量分数是![]() ;
;
故填:20%。
50℃时,甲的溶解度大于乙的溶解度,相同温度、相同质量的水中,溶解的甲的质量比乙的大,将甲、乙的饱和溶液恒温蒸发,要得到相同质量的甲、乙固体,甲需要蒸发掉的水质量小于乙要蒸发掉的水的质量;
故填:小于。
20℃时,将125g甲的饱和溶液稀释至溶质质量分数为10%的甲溶液,设需要加水的质量是X;根据溶液稀释前后,溶质的质量不变,得:
125g×20%=(125g+x)×10%
x=125g
故填:125。

【题目】在研究酸和碱的化学性质时,某小组想证明稀硫酸和氢氧化钠混合后,虽然无明显现象,但确实发生了化学反应。试与他们一起完成实验方案的设计、实施和评价,并得出有关结论。
(1)探究稀硫酸和氢氧化钠溶液的反应:
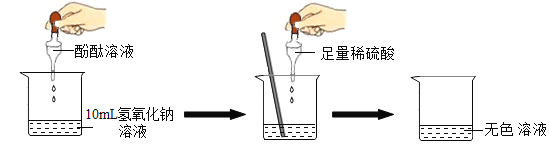
当滴入几滴酚酞溶液后,溶液由无色变为_________色。根据上述实验中颜色变化,可确定稀硫酸和氢氧化钠溶液发生了化学反应。
(2)探究上述稀硫酸和氢氧化钠溶液反应后烧杯中的硫酸是否过量:根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量。同学们又分别选取氯化钡溶液、紫色石蕊溶液设计实验方案,请你判断并(提示:Ba2+与SO42-可形成BaSO4白色沉淀)
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 有白色沉淀生成 | 稀硫酸过量 |
方案二 | 取样,滴入几滴紫色石蕊溶液 | _________ | 稀硫酸过量 |
①上述设计的实验方案中,正确的方案是:__________。
②若请你再设计一个确定稀硫酸是否过量的实验方案,你会选用的药品是_______,实验现象及结论是_____________。
(3)成成同学认为稀硫酸和氢氧化钠溶液的反应没有明显现象,他提出可以对某些有明显现象产生的中和反应进行探究,如稀盐酸和氢氧化铝的反应,可观察到的现象为_________,说明中和反应已经发生,反应的化学方程式为_______________。。(提示:氢氧化铝是不溶于水的白色固体,化学式为Al(OH)3)。
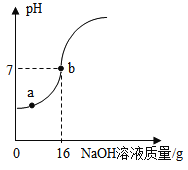
(4)现取10g一定溶质质量分数的稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。计算恰好完全反应时所得溶液的溶质质量分数______。(结果精确到0.1%)