题目内容
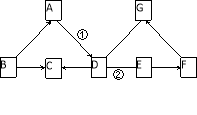
【题目】为测定实验室废液中硫酸的质量分数。小红同学做了如图所示实验,废液中其他成份不与铁粉发生反应。

请计算:
(1)反应后产生的气体的质量是 g。
(2)该废液中硫酸的质量分数。
【答案】(1)0.2 ;(2)解:设废液中硫酸的质量为x
Fe+H2SO4==FeSO4+ H2 ↑
98 2
x 0.2g
![]() x=9.8g
x=9.8g
废液中硫酸质量分数为:![]() ×100%=9.8%
×100%=9.8%
答:废液中硫酸的溶质质量分数为9.8%
【解析】
试题分析:(1)由质量守恒定律可知:完全反应后,容器中的物质的质量差,就是生成氢气的质量,氢气的质量为:100g+10g-109.8g=0.2g;(2)根据氢气的质量求出硫酸中溶质的质量,结合溶质质量分数的计算公式求出废液中硫酸的质量分数即可。

练习册系列答案
相关题目