题目内容
【题目】下图是元素周期表中的一部分。已知在元素周期表中,同一周期(横行)中的元素,除0族(最右纵行)元素外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强。请回答:
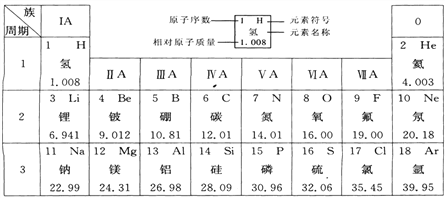
(1)从表中查出铝的相对原子质量为__________;原子序数为9的元素位于元素周期表的第_____周期,元素符号为_____,氟原子核内中子数为_______,它属于______(填“金属”或“非金属”)元素。
(2)表中不同种元素最本质的区别是_________(填序号)。
A、电子数不同 B、相对原子质量不同
C、中子数不同 D、质子数不同
(3)原子半径:钠________镁(填“>”或“==”或“<”,下同),原子得电子能力:硫________氯。
【答案】 26.98或27 二 F 10 非金属 D > <
【解析】(1)元素周期表中,元素符号下方的数字代表元素的相对原子质量,所以铝的相对原子质量为26.98或27;原子序数为9的元素即为氟元素,符号为:F,氟原子核内中子数=19-9=10,在周期表中位于第二周期,是非金属元素;(2)决定元素种类的是质子数;(3)同一周期,元素原子半径从左到右半径在减小,所以原子半径:钠>镁,同一周期,元素原子得电子能力逐渐增大,所以原子得电子能力:硫<氯。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案【题目】下列四个图像中,不能正确表示对应变化关系的是 ( )
|
|
|
|
A.向一定量稀硫酸 中加水稀释 | B.一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 | C.加热一定质量的 高锰酸钾固体 | D.向一定质量的硫酸铜和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液 |
A. A B. B C. C D. D
【题目】KCl和KNO3的溶解度表及溶解度曲线如下图所示,下列说法不正确的是 ( )
温度/℃ | 20 | 30 | 40 | 50 | |
溶解度S/g | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
A. 甲表示KCl溶解度曲线 
B. 温度t1应在20℃~30℃之间
C. 40℃时,5gKCl加入10g水中,可得到33.3%的溶液
D. 50℃时,30g KNO3加入50g水,充分溶解,再降温到30℃,有晶体析出
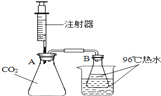
【题目】某研究性学习小组利用下图装置研究CO2与NaOH的反应。
已知:水的沸点与气体压强有关,气体压强小,沸点低;气体压强大,沸点高。
实验装置 | 实验步骤 |
| Ⅰ. A中充满CO2,B和烧杯中均盛有96℃以上但未沸腾的热水(假设实验过程无热量损耗)。 Ⅱ. 用注射器向A中注入一定量浓NaOH溶液,振荡后观察到B中热水沸腾。 Ⅲ.另取相同装置,用注射器向A中注入20mL水,振荡后观察到B中的热水没有沸腾。 |
(1)检查装置气密性:向上缓慢拉动注射器活塞至一定高度,松手后,观察到活塞_________,说明装置的气密性良好。
(2)步骤Ⅱ中注入浓NaOH溶液的体积应为_________mL。
(3)步骤Ⅲ的目的是排除_________的干扰。
(4)通过对比_________现象,可知CO2与NaOH确实发生了反应,其反应的化学方程式为_________。