题目内容
【题目】(7分)实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示).
![]()
小强和小华同学很感兴趣,决定对其成分进行探究.
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是 ( )
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ初中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3.
ⅡNa2CO3和NaHCO3的水溶液都呈碱性.
Ⅲ室温(20℃)时,测定四种物质的溶解度数据如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度g | 36 | 109 | 215 | 9.6 |
小华根据试剂瓶标注的质量分数为10%和上表中的溶解度数据判断,这瓶试剂不可能是
【作出猜想】①可能是NaCl;②可能是Na2CO3;③可能是
【实验探究】
(1)小强用洁净的玻璃棒蘸取试液于pH试纸上,测得pH>7,则这瓶试剂不可能是
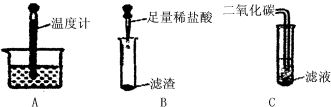
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验.
实验步骤 | 实验现象 | 结论及化学方程式 |
①取少量溶液于试管中,②滴加 | 产生大量气泡 | 反应的化学方程式: |
③把产生的气体通入澄清的石灰水中. | 澄清的石灰水变浑浊 | 猜想②正确. 反应的化学方程式: |
【答案】【交流讨论】A【查阅资料】NaHCO3 【作出猜想】NaOH
【实验探究】(1)NaCl溶液
(2)①稀盐酸 Na2CO3+2HCl=2NaCl+H2O+CO2↑
②CO2+Ca(OH)2=CaCO3↓+H2O
【解析】
试题分析:【交流讨论】通过试剂标签可以看出物质的化学式首先是钠,说明可能是碱或盐,但不能是酸,选A。【查阅资料】根据常温下碳酸氢钠的溶液为9.6克,可判断常温下碳酸氢钠的饱和溶液的溶质的质量分数=9.6/(100+9.6)=8.8%,因此可判断该溶液不可能为NaHCO3 ,而其它物质进行类似的计算都可以得到10%的溶液。【作出猜想】除碳酸氢钠外,该溶液可能是氢氧化钠或氯化钠或碳酸钠。【实验探究】(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH大于7,而氯化钠溶液呈中性,所以不可能是氯化钠。(2)①根据碳酸钠能与盐酸反应放出二氧化碳而氢氧化钠与盐酸反应无明显现象,所以可推断鉴别两物质时所加入的试剂为稀盐酸。碳酸钠与盐酸反应生成氯化钠和水和二氧化碳,方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑。②观察有气泡可说明该物质为碳酸钠,把产生的气体通入到澄清的石灰水中,石灰水变浑浊,则可进一步确定该物质,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O。

 备战中考寒假系列答案
备战中考寒假系列答案